题目内容
15.体积和pH值都相同的HCl和CH3OOH分别与足量NaHCO3反应,产生CO2的质量( )| A. | 同样多 | B. | HCl最多 | C. | 醋酸最多 | D. | 无法判断 |
分析 HCl为强酸,c(HCl)=c(H+),而CH3COOH为弱酸,其c(CH3COOH)>c(H+),c(H+)越大,与足量NaHCO3反应产生CO2的体积就越大.
解答 解:因HCl,CH3COOH为弱酸,
体积相同、pH也相同的HCl、CH3COOH溶液中,HCl的浓度等于氢离子浓度,c(CH3COOH)>c(H+),
醋酸在反应中可继续电离产生H+,最终电离生成的c(H+)最大,
则醋酸与足量NaHCO3反应产生CO2的体积最大,
故选C.
点评 本题考查弱电解质的电离平衡及其应用,题目难度不大,明确酸的酸性强弱及溶液中氢离子的浓度与pH的关系是解答本题的关键,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案
相关题目
8.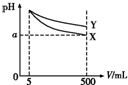 将5 mL pH=11的X、Y两种碱分别稀释至500 mL,其pH与溶液体积(V)的关系如图,下列说法正确的是( )
将5 mL pH=11的X、Y两种碱分别稀释至500 mL,其pH与溶液体积(V)的关系如图,下列说法正确的是( )
 将5 mL pH=11的X、Y两种碱分别稀释至500 mL,其pH与溶液体积(V)的关系如图,下列说法正确的是( )
将5 mL pH=11的X、Y两种碱分别稀释至500 mL,其pH与溶液体积(V)的关系如图,下列说法正确的是( )| A. | 若X、Y都是弱碱,则a的值一定大于9 | |
| B. | 完全中和X、Y两溶液时,消耗同浓度稀硫酸的体积V(X)>V(Y) | |
| C. | 稀释后X溶液中水的电离程度比Y溶液中水的电离程度小 | |
| D. | 若X、Y是一元碱,则等物质的量浓度的Y的硝酸盐溶液的pH比X的硝酸盐溶液大 |
20.下面提到的问题中,与盐的水解有关的是( )
①明矾和FeCl3可作净水剂 ②为保存FeCl3溶液,要在溶液中加少量盐酸 ③热的纯碱溶液洗涤油污的能力强 ④实验室盛放Na2CO3、Na2SiO3等溶液的试剂瓶应用橡皮塞,而不能用玻璃塞 ⑤用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂 ⑥在NH4Cl或AlCl3溶液中加入金属镁会产生氢气.
①明矾和FeCl3可作净水剂 ②为保存FeCl3溶液,要在溶液中加少量盐酸 ③热的纯碱溶液洗涤油污的能力强 ④实验室盛放Na2CO3、Na2SiO3等溶液的试剂瓶应用橡皮塞,而不能用玻璃塞 ⑤用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂 ⑥在NH4Cl或AlCl3溶液中加入金属镁会产生氢气.
| A. | ①②③④⑤ | B. | ②③⑤⑥ | C. | 全部 | D. | ①②④⑤ |
7.对于常温下0.0l mol/L的氨水,下列叙述正确的是( )
| A. | c(H+)+c(NH4+)=2c(OH-) | |
| B. | 由H2O电离出的c(H+)=1.0×10-12mol•L-1 | |
| C. | 与等体积等浓度的氯化铵溶液混合c(NH4+)+c(NH3•H2O)=0.02 mol•L-1 | |
| D. | 与等体积等浓度的盐酸混合后所得溶液c(OH-)+c(NH3•H2O)=c(H+) |