题目内容
20.下面提到的问题中,与盐的水解有关的是( )①明矾和FeCl3可作净水剂 ②为保存FeCl3溶液,要在溶液中加少量盐酸 ③热的纯碱溶液洗涤油污的能力强 ④实验室盛放Na2CO3、Na2SiO3等溶液的试剂瓶应用橡皮塞,而不能用玻璃塞 ⑤用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂 ⑥在NH4Cl或AlCl3溶液中加入金属镁会产生氢气.
| A. | ①②③④⑤ | B. | ②③⑤⑥ | C. | 全部 | D. | ①②④⑤ |
分析 ①明矾和FeCl3可作净水剂依据铝离子、铁离子水解生成胶体分析判断;
②加入盐酸抑制铁离子的水解;
③碳酸钠是强碱弱酸盐,在溶液中水解呈碱性,且盐类的水解是吸热反应,升高温度促进盐类水解;
④碳酸根、硅酸根离子水解显碱性和玻璃中的二氧化硅反应;
⑤碳酸氢根离子与铝离子发生双水解生成二氧化碳;
⑥铵根离子、铝离子水解显酸性.
解答 解:①明矾和FeCl3可作净水剂依据铝离子、铁离子水解生成胶体具有较大的表面积,具有吸附悬浮杂质的作用,故①有关;
②加入盐酸抑制铁离子的水解;Fe3++3H2O?Fe(OH)3+3H+,故②有关;
③碳酸钠是强碱弱酸盐,因为水解使其溶液呈碱性,碱能促进油脂水解,所以热纯碱溶液的洗涤油污能力强,应用了盐类水解原理,故③有关;
④碳酸根、硅酸根离子水解显碱性和玻璃中的二氧化硅反应,把玻璃瓶塞和瓶口粘结,故④有关;
⑤碳酸氢根离子与铝离子发生双水解生成二氧化碳,可以灭火,故⑤有关;
⑥铵根离子、铝离子水解显酸性,镁和氢离子反应促进水解进行生成氢气,故⑥有关;
故选C.
点评 本题考查了盐类水解的分析判断,水解离子的特征性质和溶液酸碱性的分析判断,理解盐类水解的实质是弱离子结合水中氢离子或氢氧根离子生成弱电解质,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11. 某学生用0.1000mol/L盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应).实验步骤如下:
某学生用0.1000mol/L盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应).实验步骤如下:
(1)配制待测液:用2.50g含有少量杂质的固体烧碱样品配制500mL溶液.需用的玻璃仪器除了烧杯、胶头滴管、玻璃棒外,还需要500mL容量瓶.
(2)滴定:
Ⅰ.用蒸馏水洗涤酸式滴定管,并立即注入盐酸标准溶液至“0”刻度线以上.
Ⅱ.固定好滴定管并使滴定管尖嘴充满液体,调节液面至“0”刻度线以下,并记录读数.
Ⅲ.移取20.00mL待测液注入洁净的锥形瓶中,并加入2滴酚酞试液.
Ⅳ.用标准液滴定至终点,记录滴定管液面读数.
①上述滴定步骤中有错误的是(填编号)Ⅰ.该错误操作会导致测定结果偏大(填“偏大”、“偏小”或“无影响”).
②排去碱式滴定管中气泡的方法应采用右图的丙操作.
③步骤Ⅳ中滴定时眼睛应观察锥形瓶中溶液颜色的变化;判断滴定终点的现象是当滴加最后一滴标准液时,待测液由红色刚好变为无色,且半分钟内不变色.
④若步骤Ⅱ中仰视读数,步骤Ⅳ中俯视读数,则会使测定结果偏小(填“偏大”、“偏小”或“无影响”)
(3)按正确操作测得有关数据记录如下:按正确操作测得有关数据记录如表:
①a的读数如图所示,则a=22.60; ②烧碱样品的纯度为80.8%
 某学生用0.1000mol/L盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应).实验步骤如下:
某学生用0.1000mol/L盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应).实验步骤如下:(1)配制待测液:用2.50g含有少量杂质的固体烧碱样品配制500mL溶液.需用的玻璃仪器除了烧杯、胶头滴管、玻璃棒外,还需要500mL容量瓶.
(2)滴定:
Ⅰ.用蒸馏水洗涤酸式滴定管,并立即注入盐酸标准溶液至“0”刻度线以上.
Ⅱ.固定好滴定管并使滴定管尖嘴充满液体,调节液面至“0”刻度线以下,并记录读数.
Ⅲ.移取20.00mL待测液注入洁净的锥形瓶中,并加入2滴酚酞试液.
Ⅳ.用标准液滴定至终点,记录滴定管液面读数.
①上述滴定步骤中有错误的是(填编号)Ⅰ.该错误操作会导致测定结果偏大(填“偏大”、“偏小”或“无影响”).
②排去碱式滴定管中气泡的方法应采用右图的丙操作.
③步骤Ⅳ中滴定时眼睛应观察锥形瓶中溶液颜色的变化;判断滴定终点的现象是当滴加最后一滴标准液时,待测液由红色刚好变为无色,且半分钟内不变色.
④若步骤Ⅱ中仰视读数,步骤Ⅳ中俯视读数,则会使测定结果偏小(填“偏大”、“偏小”或“无影响”)
(3)按正确操作测得有关数据记录如下:按正确操作测得有关数据记录如表:
| 滴定次数 | 待测液体积 | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.20 | 20.38 |
| 第二次 | 20.00 | 4.00 | 24.20 |
| 第三次 | 20.00 | 2.38 | a |
8.已知:25℃时,Ksp(AgCl)>Ksp(AgI),下列叙述不正确的是( )
| A. | AgI悬浊液中存在平衡:AgI(s)?Ag+(aq)+I-(aq) | |
| B. | 25℃时,向AgCl的悬浊液中加入NaCl固体,AgCl的溶度积常数不变 | |
| C. | 向含KCl、NaI的混合溶液中滴入AgNO3溶液,一定先析出AgI沉淀 | |
| D. | 用等体积的水和氯化钠溶液分别洗涤AgCl沉淀,水洗造成的AgCl损耗大 |
15.体积和pH值都相同的HCl和CH3OOH分别与足量NaHCO3反应,产生CO2的质量( )
| A. | 同样多 | B. | HCl最多 | C. | 醋酸最多 | D. | 无法判断 |
5.下列判断正确的是( )
| A. | 元素周期表中查得的相对原子质量为同使素的相对原子质量 | |
| B. | 化学键的变化一定会引起化学反应的变化 | |
| C. | 酸性氧化物一定是非金属氧化物 | |
| D. | 钢铁在海水中比在河水中更易腐蚀,主要原因是海水含氧量高于河水 |
12.下列实验过程中,始终无明显现象的是( )
| A. | 在稀硫酸中加入铜粉,再加入KNO3固体 | |
| B. | SO2通入Ba(NO3)2溶液中 | |
| C. | CO2通入CaCl2溶液中 | |
| D. | 稀盐酸滴加到Fe(OH)3胶体溶液中 |
7.下列有关物质应用的说法正确的是( )
| A. | 小苏打是面包发酵粉的主要成分之一 | |
| B. | 盐类都可用作调味品 | |
| C. | 铝罐可久盛食醋 | |
| D. | 生石灰用作食品抗氧化剂 |
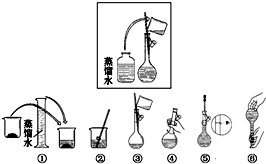 某同学帮助水质检测站配制480mL0.5mol•L-1NaOH溶液.
某同学帮助水质检测站配制480mL0.5mol•L-1NaOH溶液.