题目内容
7.对于常温下0.0l mol/L的氨水,下列叙述正确的是( )| A. | c(H+)+c(NH4+)=2c(OH-) | |
| B. | 由H2O电离出的c(H+)=1.0×10-12mol•L-1 | |
| C. | 与等体积等浓度的氯化铵溶液混合c(NH4+)+c(NH3•H2O)=0.02 mol•L-1 | |
| D. | 与等体积等浓度的盐酸混合后所得溶液c(OH-)+c(NH3•H2O)=c(H+) |
分析 A.任何电解质溶液中都存在电荷守恒,根据电荷守恒判断;
B.一水合氨是弱电解质,在溶液中部分电离,所以该溶液中c(OH-)<0.01mol/L,水电离出c(H+)=$\frac{{K}_{w}}{c(O{H}^{-})}$;
C.与等体积等浓度的氯化铵溶液混合,溶液体积增大一倍,则物质浓度降为原来的一半,再结合物料守恒判断;
D.任何溶液中都存在质子守恒,根据质子守恒判断.
解答 解:A.氨水中存在OH-、H+、NH4+,根据电荷守恒有c(H+)+c(NH4+)=c(OH-),故A错误;
B.一水合氨是弱电解质,在溶液中部分电离,所以该溶液中c(OH-)<0.01mol/L,水电离出c(H+)=$\frac{{K}_{w}}{c(O{H}^{-})}$>1.0×10-12mol•L-1,故B错误;
C.与等体积等浓度的氯化铵溶液混合溶液体积增大一倍,物质浓度降为原来的一半,结合物料守恒得c(NH4+)+c(NH3•H2O)=0.01mol•L-1,故C错误;
D.与等体积等浓度的盐酸混合后所得溶液为氯化铵溶液,其中铵根离子水解生成一水合氨和氢氧根离子,根据质子守恒,可得c(OH-)+c(NH3•H2O)=c(H+),故D正确;
故选D.
点评 本题考查弱电解质溶液中的守恒规律、氢离子浓度的计算、混合溶液的粒子浓度的判断,明确弱电解质电离特点及溶液中存在的守恒是解本题关键,易错选项是C,易忽略混合溶液体积增大而导致错误,题目难度不大.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案
相关题目
15.体积和pH值都相同的HCl和CH3OOH分别与足量NaHCO3反应,产生CO2的质量( )
| A. | 同样多 | B. | HCl最多 | C. | 醋酸最多 | D. | 无法判断 |
12.下列实验过程中,始终无明显现象的是( )
| A. | 在稀硫酸中加入铜粉,再加入KNO3固体 | |
| B. | SO2通入Ba(NO3)2溶液中 | |
| C. | CO2通入CaCl2溶液中 | |
| D. | 稀盐酸滴加到Fe(OH)3胶体溶液中 |
14.下面的原子或原子团不属于官能团的是( )
| A. | NO3- | B. | -Cl | C. | -OH | D. | 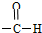 |

 ,实验中,可以观察到反应②的现象是:气体由无色变成红棕色.
,实验中,可以观察到反应②的现象是:气体由无色变成红棕色.