题目内容
下列说法中,正确的是( )
| A、在纸上层析操作时,要让试样点刚好接触展开剂,否则不能很好地分离 |
| B、实验室制备硝基苯时,先将浓硫酸滴入浓硝酸后,冷却,再边振荡边滴加苯 |
| C、从海带中提取碘的方法是:取样→灼烧→溶解→过滤→萃取 |
| D、向盛有少量Na2O2的试管中加入少量水,并立即滴入2滴酚酞,振荡,溶液呈红色 |
考点:化学实验方案的评价,苯的性质,物质的分离、提纯的基本方法选择与应用,海带成分中碘的检验,碱金属及其化合物的性质实验
专题:实验评价题
分析:A.纸上层析操作时,不让试样点接触展开剂;
B.制备硝基苯,防止苯挥发,提高原料利用率;
C.碘以离子形成存在,应加氧化剂氧化;
D.滴入2滴酚酞,先变红后褪色.
B.制备硝基苯,防止苯挥发,提高原料利用率;
C.碘以离子形成存在,应加氧化剂氧化;
D.滴入2滴酚酞,先变红后褪色.
解答:
解:A.纸上层析中要求流动相溶剂对分离物质应有适当的溶解度,由于样品中各物质分配系数不同,因而扩散速度不同,所以纸上层析法是利用试样中各种离子随展开剂在滤纸上展开的速率不同而形成不同位置的色斑,如果试样接触展开剂,样点里要分离的离子或者色素就会进入展开剂,导致实验失败,故A错误;
B.制备硝基苯,防止苯挥发,提高原料利用率,则先将浓硫酸滴入浓硝酸后,冷却,再边振荡边滴加苯来制备硝基苯,故B正确;
C.碘以离子形成存在,应加氧化剂氧化,则从海带中提取碘的方法是:取样→灼烧→溶解→过滤→氧化→萃取,故C错误;
D.滴入2滴酚酞,过氧化钠与水反应生成碱先变红,过量过氧化钠具有强氧化性,后褪色,故D错误;
故选B.
B.制备硝基苯,防止苯挥发,提高原料利用率,则先将浓硫酸滴入浓硝酸后,冷却,再边振荡边滴加苯来制备硝基苯,故B正确;
C.碘以离子形成存在,应加氧化剂氧化,则从海带中提取碘的方法是:取样→灼烧→溶解→过滤→氧化→萃取,故C错误;
D.滴入2滴酚酞,过氧化钠与水反应生成碱先变红,过量过氧化钠具有强氧化性,后褪色,故D错误;
故选B.
点评:本题考查化学实验方案的评价,为高频考点,涉及混合物分离提纯、物质制备、海水资源利用及过氧化钠的性质等,侧重物质性质及实验操作的考查,注意实验方案的评价性、操作性分析,题目难度不大.

练习册系列答案
相关题目
在一个不传热的固定容积的密闭容器中,可逆反应N2(气)+3H2(气)?2NH3(气),达到平衡的标志是:①反应速率υ(N2):υ(H2):υ(NH3)=1:3:2;②各组分的物质的量浓度不再改变;③体系的压强不再发生变化;④混合气体的密度不变(相同状况);⑤体系的温度不再发生变化;⑥2υ(N2)(正反应)=υ(NH3)(逆反应)⑦单位时间内3molH-H断键反应同时2molN-H也断键反应( )
| A、①②③⑤⑥ | B、②③④⑤⑥ |
| C、②③④⑥⑦ | D、②③⑤⑥ |
同温同压下,A容器中氯化氢与B容器中氨气所含原子数相等,两容器体积之比为( )
| A、1:4 | B、2:1 |
| C、1:2 | D、4:1 |
下列叙述表示可逆反应N2+3H2?2NH3一定处于平衡状态的是( )
| A、N2、H2、NH3的百分含量相等 |
| B、3v(N2)正=v(H2)逆 |
| C、定容容器中,气体的密度不变 |
| D、N2、H2、NH3的浓度之比为1:3:2 |
在含有n mol FeI2的溶液中通入Cl2,有x mol Cl2发生反应.下列说法正确的是( )
A、当x≤
| ||
| B、当x≥n时,反应的离子方程式为:2Fe2++2I-+2Cl2→2Fe3++I2+4Cl- | ||
| C、当Fe2+和I-都被氧化时,x与n的关系为x>n | ||
| D、当x=n时,反应后氧化产物的物质的量为n mol |
已知在常温下测得浓度均为0.1mol/L的下列6种溶液的pH值:
下列说法或表达中,正确的是( )
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
| A、少量二氧化碳通入NaClO溶液中:2NaClO+CO2+H2O→Na2CO3+2HClO |
| B、过量的 HCN滴入碳酸钠溶液中 HCN+Na2CO3→NaCN+NaHCO3 |
| C、结合质子能力由强到弱的顺序为:CO32->CN->HCO3->CH3COO- |
| D、常温下电离常数:Ki2(H2CO3)>Ki(C6H5OH)>Ki(HCN) |
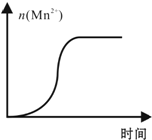 KMnO4酸性溶液与草酸(H2C2O4)溶液反应时,溶液紫色会逐渐褪去.某探究小组用测定此反应溶液紫色消失所需时间的方法,研究外界条件对反应速率的影响.该实验条件作如下限定:
KMnO4酸性溶液与草酸(H2C2O4)溶液反应时,溶液紫色会逐渐褪去.某探究小组用测定此反应溶液紫色消失所需时间的方法,研究外界条件对反应速率的影响.该实验条件作如下限定: