题目内容
16.足量的下列物质与相同质量的铝反应,放出氢气且消耗溶质物质的量最少的是( )| A. | 稀硝酸 | B. | 稀硫酸 | C. | 盐酸 | D. | 氢氧化钠溶液• |
分析 结合2Al~2NaOH~3H2SO4~6HCl计算,Al与稀硝酸不生成氢气,以此来解答.
解答 解:设Al均为2mol,则
A.Al与稀硝酸不生成氢气;
B.由2Al~3H2SO4可知,生成氢气,且消耗3molH2SO4;
C.由2Al~6HCl可知,生成氢气,且消耗6molHCl;
D.由2Al~2NaOH可知,生成氢气,且消耗2molNaOH;
所以消耗的溶质最少的是NaOH溶液.
故选D.
点评 本题考查Al的化学性质,把握铝与酸、碱发生的化学反应为解答的关键,侧重金属化学性质的考查,题目难度不大.

练习册系列答案
相关题目
6.下列物质放入水中,会显著放热的是( )
| A. | 生石灰 | B. | 硝酸铵 | C. | 氯化钠 | D. | 蔗糖 |
11.关于${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、${\;}_{1}^{3}$H、H+、${\;}_{1}^{1}$H2、${\;}_{1}^{2}$H2的说法,正确的是( )
| A. | 是氢元素的五种核素 | |
| B. | ${\;}_{1}^{1}$H2、${\;}_{1}^{2}$H2互称为同素异形体 | |
| C. | ${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、${\;}_{1}^{3}$H互称为同位素 | |
| D. | ${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、${\;}_{1}^{3}$H的化学性质不同 |
1.下列说法正确的是( )
| A. | 聚乙烯塑料的老化是因为发生了加成反应 | |
| B. | 利用粮食酿酒经历了淀粉→葡萄糖→乙醇的化学变化过程 | |
| C. | 淀粉、油脂、蛋白质在-定条件下都能发生水解反应 | |
| D. | 石油的分馏和煤的干馏都是发生了化学变化 |
8.青蒿酸(简式如图所示)可用作合成青蒿素的原料,下列关于青蒿酸的说法中正确的是( )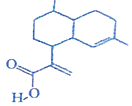

| A. | 该物质属于芳香族化合物 | B. | 该物质易溶于水 | ||
| C. | 能发生取代反应和加成反应 | D. | 分子中所有碳原子可能共平面 |
5.下列离子方程式表达正确的是( )
| A. | Na2S的水解:S2ˉ+2H2O?H2S+2OHˉ | |
| B. | 将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 硫酸亚铁酸性溶液中加入过氧化氢:2Fe2++H2O2+2H+=2Fe3++2H2O | |
| D. | 向NaClO溶液中通入少量SO2:2ClOˉ+SO2+H2O=SO32ˉ+2HClO |
16. 已知五种短周期元素在周期表中的相对位置如表所示.
已知五种短周期元素在周期表中的相对位置如表所示.
(1)表中五种元素金属性最强的元素为Na(填元素符号),c、e两元素形成的离子化合物c2e的电子式为 .
.
(2)c、d、e三种元素的简单离子中,半径最小的是Al3+(用元素符号表示).
(3)b、e两元素分别与a形成的最简单气态化合物的稳定性的关系为H2O>H2S(或H2S<H2O)(用化学式表示).
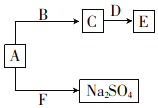
(4)已知A、B、C、D、E、F六种化合物均由上述元素中的几种组成.它们之间的关系如图所示,A为淡黄色固体,B是常见液体,D是两性氧化物,F是引起酸雨的主要气体.
①写出物质E的化学式:NaAlO2.
②写出A与F反应的化学方程式:Na2O2+SO2=Na2SO4.
 已知五种短周期元素在周期表中的相对位置如表所示.
已知五种短周期元素在周期表中的相对位置如表所示.| a | |||||
| b | |||||
| c | d | e |
 .
.(2)c、d、e三种元素的简单离子中,半径最小的是Al3+(用元素符号表示).
(3)b、e两元素分别与a形成的最简单气态化合物的稳定性的关系为H2O>H2S(或H2S<H2O)(用化学式表示).
(4)已知A、B、C、D、E、F六种化合物均由上述元素中的几种组成.它们之间的关系如图所示,A为淡黄色固体,B是常见液体,D是两性氧化物,F是引起酸雨的主要气体.
①写出物质E的化学式:NaAlO2.
②写出A与F反应的化学方程式:Na2O2+SO2=Na2SO4.
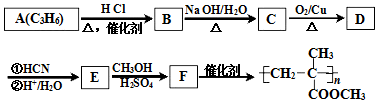
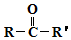 $→_{②H+/H_{2}O}^{①HCN}$
$→_{②H+/H_{2}O}^{①HCN}$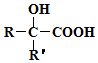 (R'可以是烃基,也可以是H原子)
(R'可以是烃基,也可以是H原子)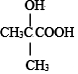 ,2分子E在浓硫酸、加热的条件下可以生成一种含六元环的化合物,该化合物的结构简式为
,2分子E在浓硫酸、加热的条件下可以生成一种含六元环的化合物,该化合物的结构简式为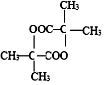 .
. )的合成路线(无机试剂可以任选)
)的合成路线(无机试剂可以任选)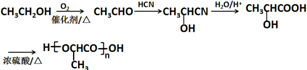 .
.