题目内容
5.铁钉溶于稀盐酸后,加入过量氢氧化钠溶液,然后放置于空气中一段时间,此时铁的存在形式为( )| A. | Fe(OH)3 | B. | Fe(OH)2 | C. | FeCl2 | D. | FeCl3 |
分析 铁钉溶于稀盐酸后 发生反应生成氯化亚铁和氢气,加入过量氢氧化钠溶液发生反应生成氢氧化亚铁白色沉淀,然后放置于空气中一段时间,迅速变化为灰绿色最后变化为红褐色.
解答 解:铁钉溶于稀盐酸后 发生反应生成氯化亚铁和氢气,Fe+2HCl=FeCl2+H2↑,加入过量氢氧化钠溶液发生反应生成氢氧化亚铁白色沉淀,FeCl2+2NaOH=Fe(OH)2↓+2NaCl,然后放置于空气中一段时间,迅速变化为灰绿色最后变化为红褐色,4Fe(OH)2+O2+2H2O=4Fe(OH)3,此时铁的存在形式为Fe(OH)3,
故选A.
点评 本题考查了铁及其化合物性质,主要是氢氧化亚铁制备和氢氧化铁生成的分析,反应现象是解题关键,题目难度不大.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
7.同位素示踪法可用于反应机理的研究,下列反应中同位素示踪表示正确的是( )
| A. | CH3COOH+CH3CH218OH═CH3COOCH2CH3+H218O | |
| B. | K37ClO3+6HCl═K37Cl+3Cl2↑+3H2O | |
| C. | 2Na218O2+2H2O═4Nal8OH+O2↑ | |
| D. | 2KMnO4+5H218O2+3H2SO4═K2SO4+2MnSO4+518O2↑+8H2O |
8.下列说法正确的是( )
| A. | 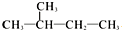 与 与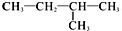 互为同分异构体 互为同分异构体 | |
| B. | CH3-CH2-CH3、CH3-CH2-CH2-CH2-CH3、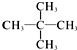 互为同系物,熔沸点逐渐升高 互为同系物,熔沸点逐渐升高 | |
| C. | 烷烃燃烧通式为:CnH2n+2+$\frac{3n+1}{2}$O2$\stackrel{点燃}{→}$nCO2+(n+1)H2O | |
| D. | 分子式为C4H10O并能与金属钠反应放出氢气的有机物有3种 |
17.能正确表示下列反应的离子方程式的是( )
| A. | 硅酸钠溶液中通入过量的CO2:SiO32-+CO2+H2O═H2SiO3↓+CO32- | |
| B. | 将FeCl3饱和溶液滴入沸水中制取Fe(OH)3胶体:Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3H+ | |
| C. | 向NaHSO4溶液中加入过量的Ba(OH)2溶液:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| D. | 向0.1mol/L、pH=1的NaHA溶液中加入NaOH溶液:HA-+OH-═A2-+H2O |
15.下列对事故的处理方法中不正确的是( )
| A. | 当液氯罐破损时,为防止液氯泄漏,立即将罐置于碱水池中进行处理 | |
| B. | 不小心将苯酚沾到手上,用酒精洗涤 | |
| C. | 实验桌上酒精灯被碰翻而引起少量酒精着火,用湿布盖灭 | |
| D. | 金属钠着火时,用泡沫灭火器灭火 |
 具有水果香味的中性物质A可以发生下列变化:
具有水果香味的中性物质A可以发生下列变化: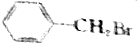 ②CH3CH2CH3Br ③CH3Br ④CH3CHBrCH2CH3
②CH3CH2CH3Br ③CH3Br ④CH3CHBrCH2CH3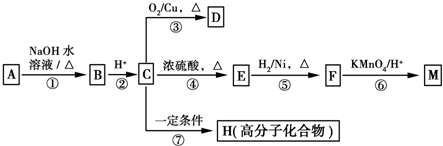
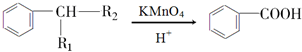 (R1、R2表示烃基或氢原子)
(R1、R2表示烃基或氢原子)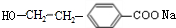 .
.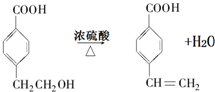 .
. .
.