题目内容
8.下列说法正确的是( )| A. | 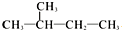 与 与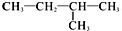 互为同分异构体 互为同分异构体 | |
| B. | CH3-CH2-CH3、CH3-CH2-CH2-CH2-CH3、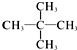 互为同系物,熔沸点逐渐升高 互为同系物,熔沸点逐渐升高 | |
| C. | 烷烃燃烧通式为:CnH2n+2+$\frac{3n+1}{2}$O2$\stackrel{点燃}{→}$nCO2+(n+1)H2O | |
| D. | 分子式为C4H10O并能与金属钠反应放出氢气的有机物有3种 |
分析 A.分子式、结构均相同;
B.CH3-CH2-CH2-CH2-CH3、 的分子式相同,结构不同;
的分子式相同,结构不同;
C.燃烧生成二氧化碳和水,遵循质量守恒定律;
D.分子式为C4H10O并能与金属钠反应放出氢气为醇,-C4H10有4种.
解答 解:A.分子式、结构均相同,则二者为同种物质,故A错误;
B.CH3-CH2-CH2-CH2-CH3、 的分子式相同,结构不同,二者互为同分异构体,且支链多的沸点低,故B错误;
的分子式相同,结构不同,二者互为同分异构体,且支链多的沸点低,故B错误;
C.燃烧生成二氧化碳和水,CnH2n+2+$\frac{3n+1}{2}$O2$\stackrel{点燃}{→}$nCO2+(n+1)H2O遵循质量守恒定律,故C正确;
D.分子式为C4H10O并能与金属钠反应放出氢气为醇,-C4H10有4种,满足条件的有机物有4种,故D错误;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意同系物、同分异构体的判断,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.下面实验操作不能实现实验目的是( )
| 实验操作 | 目的 | |
| A | 取绿豆大的钠分别加入到水和乙醇中 | 证明乙醇羟基中氢原子不如水分 子中氢原子活泼 |
| B | 取绿豆大的钠与钾分别投入水中 | 证明钾的金属性强于钠 |
| C | 将石蜡油在催化作用下,加强热产生的气 体通入溴的四氯化碳溶液中 | 证明产物不都是烷烃 |
| D | 加热乙酸乙酯、乙醇和乙酸的混合物 | 除去乙酸乙酯中的乙醇和乙酸 |
| A. | A | B. | B | C. | C | D. | D |
16.在一定温度下,向一个2L的真空密闭容器中(预先装入催化剂)通入1mol N2和3mol H2,经过一段时间后,测得容器内压强与起始时的压强之比为9:10.在此时间内H2的平均反应速率为0.1mol•(L•min)-1,则经过时间为( )
| A. | 2 min | B. | 3 min | C. | 4 min | D. | 5 min |
3.25℃的下列溶液中,碱性最强的是( )
| A. | 1L中含有4 g NaOH的溶液 | |
| B. | 稀释1mL,1mol/L NaOH溶液到1L后所得溶液 | |
| C. | pH=11的溶液 | |
| D. | 0.11 mol/LNaOH溶液跟等体积0.05mol/L H2SO4溶液的混合液 |
13.氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛用于电子工业、陶瓷工业等领域.在一定条件下,氮化铝可通过反应 Al2O3+N2+3C═2AlN+3CO合成,下列叙述正确是( )
| A. | 反应中,N2是还原剂,Al2O3是氧化剂 | |
| B. | 反应中,每生成2 mol AlN,N2得到3 mol电子 | |
| C. | 氮化铝中氮元素的化合价为-3 | |
| D. | AlN的摩尔质量为41g |
5.铁钉溶于稀盐酸后,加入过量氢氧化钠溶液,然后放置于空气中一段时间,此时铁的存在形式为( )
| A. | Fe(OH)3 | B. | Fe(OH)2 | C. | FeCl2 | D. | FeCl3 |
6.下面是生产生活中的常见 有机物的分子式、结构(简)式或名称:① ②
②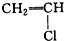 ③
③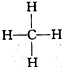 ④
④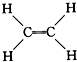 ⑤CH3CH2OH,⑥C6H12O6,⑦CH3COOH,⑧硬脂酸甘油酯,⑨聚乙烯
⑤CH3CH2OH,⑥C6H12O6,⑦CH3COOH,⑧硬脂酸甘油酯,⑨聚乙烯
下列有关说法正确的是( )
 ②
②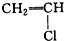 ③
③ ④
④ ⑤CH3CH2OH,⑥C6H12O6,⑦CH3COOH,⑧硬脂酸甘油酯,⑨聚乙烯
⑤CH3CH2OH,⑥C6H12O6,⑦CH3COOH,⑧硬脂酸甘油酯,⑨聚乙烯下列有关说法正确的是( )
| A. | 能与溴的四氯化碳溶液发生加成反应并使之褪色的有①②④⑨ | |
| B. | 投入钠能产生H2的是⑤⑦⑧ | |
| C. | 属于高分子材料的是⑧⑨ | |
| D. | 既能和NaOH溶液反应又能与NaHCO3溶液反应的是 ⑦ |