题目内容
20. 在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
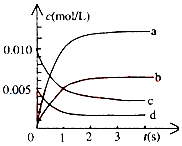
(2)图中表示NO2的变化的曲线是b,用O2表示从0~2s内该反应的平均速率v(O2)=0.0015mol/(L•s).
(3)能说明该反应已经达到平衡状态的是BC.
A.单位时间内消耗a mol NO,同时生成a mol NO2
B.容器内压强保持不变
C.v逆(NO)=2v正(O2)
D.容器内的密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是C.
A.及时分离出NO2气体 B.适当升高温度
C.增大O2的浓度 D.选择高效的催化剂.
分析 (1)化学平衡常数,是指在一定温度下,可逆反应都达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,据此书写;达平衡时,NO的转化率等于消耗量除以起始量,K(300℃)>K(350℃),说明升高温度平衡向逆反应移动,故正反应是放热反应;
(2)由表中数据可知,平衡时c(NO)=$\frac{0.007mol}{2}$=0.0035mol/L,由方程式2NO(g)+O2(g)?2NO2(g)可知,平衡时△c(NO):△c(O2):△c(NO2)=2:1:2,据此判断表示NO2的浓度变化的曲线,由图中数据可知2s内,NO的浓度变化量为0.01mol/L-0.004mol/L=0.006mol/L,根据v=$\frac{△c}{△t}$计算v(NO),再根据速率之比等于化学计量数之比计算v(O2);
(3)根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态;
(4)根据外界条件对反应速率与平衡的移动分析解答.
解答 解:(1)可逆反应2NO(g)+O2(g)?2NO2(g)的平衡常数k=$\frac{{c}^{2}(N{O}_{2})}{{c}^{2}(NO)c({O}_{2})}$,
图表中NO起始量为0.020mol,达平衡时物质的量为0.0070mol,NO的转化率=$\frac{0.020mol-0.0070mol}{0.020mol}$×100%=65%,
K(300℃)>K(350℃),说明升高温度平衡向逆反应移动,故正反应是放热反应,
故答案为:$\frac{{c}^{2}(N{O}_{2})}{{c}^{2}(NO)c({O}_{2})}$;65%;放热;
(2)由方程式2NO(g)+O2(g)?2NO2(g)可知,平衡时△c(NO):△c(O2):△c(NO2)=2:1:2,由表中数据可知,平衡时△c(NO)=$\frac{0.02mol-0.007mol}{2L}$=0.00625mol/L,曲线b平衡时的浓度为0.00625mol/L,故曲线b表示NO2的浓度变化,
由图中数据可知2s内,NO的浓度变化量为0.01mol/L-0.004mol/L=0.006mol/L,故v(NO)=$\frac{0.006mol/L}{2s}$=0.003mol/(L•s),根据速率之比等于化学计量数之比,故v(O2)=$\frac{1}{2}$v(NO)=$\frac{1}{2}$×0.003mol/(L•s)=0.0015mol/(L•s),
故答案为:b;0.0015mol/(L•s);
(3)A.单位时间内消耗a mol NO,同时生成a mol NO2,只能说明反应正向进行,故不能说明到达平衡,故A错误;
B.随反应进行气体的物质的量减小,压强增减小,容器内压强保持不变,说明到达平衡,故B正确;
C.不同物质表示的正逆速率之比等于化学计量数之比,反应到达平衡,故v逆(NO)=2v正(O2),说明到达平衡,故C正确;
D.反应混合气体的质量不变,容器的体积不变,密度始终不变,故容器内物质的密度保持不变,不能说明到达平衡,故D错误;
故选BC,
故答案为:BC;
(4)A.及时分离出NO2气体,平衡向正反应移动,但反应速率降低,故A错误;
B.适当升高温度,反应速率增大,平衡向逆反应移动,故B错误;
C.增大O2的浓度,反应速率增大,平衡向正反应移动,故C正确;
D.选择高效的催化剂,增大反应速率,不影响平衡移动,故D错误;
故选C,
故答案为:C.
点评 本题考查平衡常数即影响因素、化学反应速率、影响化学平衡的元素与平衡状态的判断等,难度中等,注意平衡状态判断选择判断的物理量,应随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.

 通城学典默写能手系列答案
通城学典默写能手系列答案| A. | Al3+、CH3COO-、Cl- | B. | Mg2+、Ba2+、Br- | ||
| C. | Mg2+、Cl-、I- | D. | Na+、NH4+、Cl- |
| A. | 反应中硫酸作氧化剂 | |
| B. | NH4CuSO3中硫元素被氧化 | |
| C. | 刺激性气味的气体是氨气 | |
| D. | 1mol NH4CuSO3完全反应转移0.5mol电子 |
| A. | 100 mL | B. | 250 mL | C. | 400 mL | D. | 1000 mL |
| A. | 46g NO2和N2O4混合气体中含有原子数为3NA | |
| B. | 标准状况下22.4 L HF中含原子数为2NA | |
| C. | 1L 1mol/L醋酸溶液中离子总数为2NA | |
| D. | 7.1g氯气与足量NaOH溶液反应转移的电子数为0.2NA |
| A. | 甲烧杯中放入锌的质量比乙烧杯中放入锌的质量大 | |
| B. | 甲烧杯中的酸过量 | |
| C. | 甲烧杯比乙烧杯反应快 | |
| D. | 反应开始后乙烧杯中的c(H+)始终比甲烧杯中的c(H+)小 |
| A. | 蔗糖 | B. | 二氧化硫 | C. | 水 | D. | 镁条 |
| A. | 饱和Na2CO3溶液 | B. | 石灰水 | C. | CaCl2溶液 | D. | Ba(OH)2溶液 |
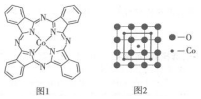 根据所学的物质结构的相关知识回答下列问题:
根据所学的物质结构的相关知识回答下列问题: