题目内容
11.已知NH4CuSO3与足量的1mol•L-1硫酸溶液混合微热,产生下列现象:①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色.据此判断下列说法正确的是( )| A. | 反应中硫酸作氧化剂 | |
| B. | NH4CuSO3中硫元素被氧化 | |
| C. | 刺激性气味的气体是氨气 | |
| D. | 1mol NH4CuSO3完全反应转移0.5mol电子 |
分析 NH4CuSO3与硫酸混合微热,生成红色固体物、产生有刺激性气味的气体和蓝色溶液,说明反应生成Cu、SO2和Cu2+,反应的方程式为:2NH4CuSO3+4H+═Cu+Cu2++2SO2↑+2H2O+2NH4+,则NH4CuSO3中Cu的化合价为+1价,以此解答该题.
解答 解:A、由方程式为:2NH4CuSO3+4H+═Cu+Cu2++2SO2↑+2H2O+2NH4+,反应只有Cu元素的化合价发生变化,硫酸根反应前后未变,反应中硫酸体现酸性,不作氧化剂,故A错误;
B、NH4CuSO3与硫酸混合微热,生成红色固体物、产生有刺激性气味的气体和蓝色溶液,说明反应生成Cu、SO2和Cu2+,反应前后S元素的化合价没有发生变化,故B错误;
C、因反应是在酸性条件下进行,不可能生成氨气,故C错误;
D、反应只有Cu元素的化合价发生变化,分别由+1→+2,+1→0,反应的发产生为:2NH4CuSO3+4H+═Cu+Cu2++2SO2↑+2H2O+2NH4+,每2molNH4CuSO3参加反应则转移1mol电子,则1molNH4CuSO3完全反应转移0.5mol电子,故D正确.
故选:D.
点评 本题考查氧化还原反应,难度较大,注意从反应现象判断生成物,结合化合价的变化计算电子转移的数目.

练习册系列答案
相关题目
19.在11g某化合物X2S中.含S2-离子3.2g.则X的相对原子质量为( )
| A. | 23 | B. | 24 | C. | 39 | D. | 40 |
6.下列实验操作正确的是( )
| A. | 蒸发:应使混合物中的水分完全蒸干后,才能停止加热 | |
| B. | 蒸馏:开始蒸馏时应先加热再开冷凝水;蒸馏完毕,应先关冷凝水再撤酒精灯 | |
| C. | 分液:下层液体从分液漏斗下口放出后,再将上层液体从下口放出到另一烧杯 | |
| D. | 量取:用规格为10mL的量筒量取8.0mL液体 |
20.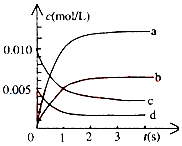 在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
(1)写出该反应的平衡常数表达式:K=$\frac{{c}^{2}(N{O}_{2})}{{c}^{2}(NO)c({O}_{2})}$,计算:达平衡时,NO的转化率=65%,已知:K(300℃)>K(350℃),该反应是放热反应.(填“放热”或“吸热”)
(2)图中表示NO2的变化的曲线是b,用O2表示从0~2s内该反应的平均速率v(O2)=0.0015mol/(L•s).
(3)能说明该反应已经达到平衡状态的是BC.
A.单位时间内消耗a mol NO,同时生成a mol NO2
B.容器内压强保持不变
C.v逆(NO)=2v正(O2)
D.容器内的密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是C.
A.及时分离出NO2气体 B.适当升高温度
C.增大O2的浓度 D.选择高效的催化剂.
 在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)图中表示NO2的变化的曲线是b,用O2表示从0~2s内该反应的平均速率v(O2)=0.0015mol/(L•s).
(3)能说明该反应已经达到平衡状态的是BC.
A.单位时间内消耗a mol NO,同时生成a mol NO2
B.容器内压强保持不变
C.v逆(NO)=2v正(O2)
D.容器内的密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是C.
A.及时分离出NO2气体 B.适当升高温度
C.增大O2的浓度 D.选择高效的催化剂.
10.在下列烷烃中,含碳量最高的是( )
| A. | 甲烷 | B. | 乙烷 | C. | 己烷 | D. | 十七烷 |