题目内容
9.下列属于电解质的是( )| A. | 蔗糖 | B. | 二氧化硫 | C. | 水 | D. | 镁条 |
分析 在水溶液里或熔融状态下能导电的化合物是电解质,电解质首先必须是化合物,根据定义分析解答.
解答 解:A.蔗糖的水溶液或熔融状态都不导电,所以蔗糖是非电解质,故A错误;
B.二氧化硫本身不能电离出离子,属于非电解质,故B错误;
C.水能电离出离子微弱的导电,所以水是电解质,故C正确;
D.镁条为金属单质,既不是电解质也不是非电解质,故D错误;
故选C.
点评 本题考查了电解质的判断,注意电解质是指化合物,水溶液中或熔融状态下导电是判断依据,题目难度不大.

练习册系列答案
 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
19.在11g某化合物X2S中.含S2-离子3.2g.则X的相对原子质量为( )
| A. | 23 | B. | 24 | C. | 39 | D. | 40 |
20.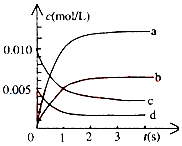 在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
(1)写出该反应的平衡常数表达式:K=$\frac{{c}^{2}(N{O}_{2})}{{c}^{2}(NO)c({O}_{2})}$,计算:达平衡时,NO的转化率=65%,已知:K(300℃)>K(350℃),该反应是放热反应.(填“放热”或“吸热”)
(2)图中表示NO2的变化的曲线是b,用O2表示从0~2s内该反应的平均速率v(O2)=0.0015mol/(L•s).
(3)能说明该反应已经达到平衡状态的是BC.
A.单位时间内消耗a mol NO,同时生成a mol NO2
B.容器内压强保持不变
C.v逆(NO)=2v正(O2)
D.容器内的密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是C.
A.及时分离出NO2气体 B.适当升高温度
C.增大O2的浓度 D.选择高效的催化剂.
 在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)图中表示NO2的变化的曲线是b,用O2表示从0~2s内该反应的平均速率v(O2)=0.0015mol/(L•s).
(3)能说明该反应已经达到平衡状态的是BC.
A.单位时间内消耗a mol NO,同时生成a mol NO2
B.容器内压强保持不变
C.v逆(NO)=2v正(O2)
D.容器内的密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是C.
A.及时分离出NO2气体 B.适当升高温度
C.增大O2的浓度 D.选择高效的催化剂.
17.依据图判断,下列说法不正确的是( )
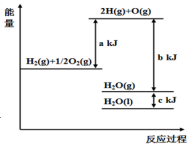

| A. | 1 mol H2(g)与$\frac{1}{2}$ mol O2(g)所具有的总能量比1 mol H2O(g)所具有的总能量高 | |
| B. | H2O(g)生成H2O(l)时,断键吸收的能量小于成键放出的能量 | |
| C. | 2 mol H(g)与1 mol O(g)生成1 molH2O(g)所放出的热量是b kJ | |
| D. | 液态水分解的热化学方程式为:2H2O(l)═2H2(g)+O2(g)△H=2(b+c-a)kJ•mol-1 |
4.在一个10L的密闭容器发生反应A(g)+B(g)?C(g)+D(g),测得平衡常数和温度的关系如表:
回答下列问题:
(1)△H< 0(填“<”或“>”).
(2)830℃时,向一个10L的密闭容器中充入1mol的A和1mol的B,则:
①反应达平衡时,n (D)=0.5mol,则A的平衡转化率为50%,
②该温度下平衡常数K=1.
(3)判断该反应是否达到平衡的依据为ad
a.c(A)不再改变 b.混合气体的密度不再改变
c.体系内压强不再改变 d.单位时间内生成C和消耗D的物质的量相等
(4)1200℃时反应C(g)+D(g)?A(g)+B(g)的平衡常数为2.5.
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | K | 0.6 | 0.4 |
(1)△H< 0(填“<”或“>”).
(2)830℃时,向一个10L的密闭容器中充入1mol的A和1mol的B,则:
①反应达平衡时,n (D)=0.5mol,则A的平衡转化率为50%,
②该温度下平衡常数K=1.
(3)判断该反应是否达到平衡的依据为ad
a.c(A)不再改变 b.混合气体的密度不再改变
c.体系内压强不再改变 d.单位时间内生成C和消耗D的物质的量相等
(4)1200℃时反应C(g)+D(g)?A(g)+B(g)的平衡常数为2.5.
10.在下列烷烃中,含碳量最高的是( )
| A. | 甲烷 | B. | 乙烷 | C. | 己烷 | D. | 十七烷 |
8.工业上可以利用水煤气(H2、CO)合成二甲醚(CH3OCH3),同时生成CO2.
2H2(g)+CO(g)═CH3OH(g)△H=-91.8kJ/mol
2CH3OH(g)═CH3OCH3 (g)+H2O(g)△H=-23.5kJ/mol
CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41.3kJ/mol
下列说法不正确的是( )
2H2(g)+CO(g)═CH3OH(g)△H=-91.8kJ/mol
2CH3OH(g)═CH3OCH3 (g)+H2O(g)△H=-23.5kJ/mol
CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41.3kJ/mol
下列说法不正确的是( )
| A. | 二甲醚与乙醇互为同分异构体 | |
| B. | CH3OCH3中只含有极性共价键 | |
| C. | CH3OH和乙醇均可发生消去反应 | |
| D. | 水煤气合成二甲醚的热化学方程式:3H2(g)+3CO(g)═CH3OCH3 (g)+CO2(g)△H=-248.4kJ/mol |