��Ŀ����
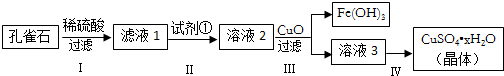
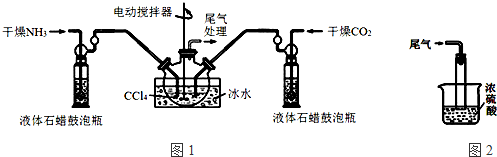
7������������泥�NH2COONH4�����Ʊ������������һ�ְ�ɫ���壬�ֽ⡢��ˮ�⣬������CCl4�����������ϣ��Ʊ���������淋�װ����ͼ1��ʾ����Ӧ�Ļ�ѧ����ʽ���£�2NH3��g��+CO2��g��?NH2COONH4��s����H��0��
ע�����Ȼ�̼��Һ��ʯ����Ϊ���Խ��ʣ�
��1���������ñ�ˮ��ȴ��ԭ���ǽ����¶ȣ���߷�Ӧ��ת���ʣ����¶ȣ���ֹ��Ӧ������ɲ���ֽ⣩��
��2��Һ��ʯ������ƿ��������ͨ���۲����ݣ�����NH3��CO2ͨ�������
��3���ӷ�Ӧ��Ļ�����з������Ʒ��ʵ�鷽���ǹ��ˣ���д�������ƣ���Ϊ�˵õ������Ʒ��Ӧ��ȡ�ķ�����C����дѡ����ţ���
a.80���ȷ��º�� b.60���ȷ��º�� c.40���ȷ��º��
��4��β������װ����ͼ2��ʾ��˫ͨ�����ܵ����ã���ֹ������Ũ��������ã����ն��ఱ������ֹ������ˮ�������뷴Ӧ��ʹ���������ˮ�⣮
��5��ȡ�ֱ��ʶ�����̼����淋İ����������Ʒ0.7820g��������ʯ��ˮ��ִ�����ʹ̼Ԫ����ȫת��Ϊ̼��ƣ����ˡ�ϴ�ӡ�����������Ϊ1.000g������Ʒ�а�������淋����ʵ�������Ϊ80%������ȷ��2λС����̼����狀Ͱ�������淋���Է��������ֱ�Ϊ79��78��
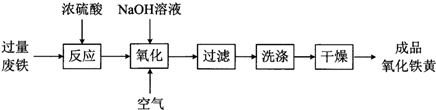
���� FeSO4•7H2O������Ʊ�
��6����֪��
| �������� | ��ʼ������pH | ������ȫ��pH |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
����һ���������м���������ϡ�����ַ�Ӧ����ַ�Ӧ����ˣ�
������Һ�м������������ۣ�
�۹��ˣ���Һ�еμ�NaOH��Һ���ڷ�ӦҺ��pHԼΪ5�����ˣ�
�ܽ��õ���Һ��������Ũ������ȴ�ᾧ�����ˣ�ϴ�ӣ����¸���õ�FeSO4•7H2O���壮
���� ��1���˷�Ӧ�ǿ��淴Ӧ������Ӧ�Ƿ��ȷ�Ӧ�����ƽ���ƶ����ۣ�Ϊ��߷�Ӧ���ת���ʣ��轵�´�ƽ��������У�����ҲҪ���Dz���IJ��ȶ��ԣ����¿ɱ������ֽ⣻
��2��Һ��ʯ������ƿ����Ҫ�����ǿ��Ʒ�Ӧ���г̶ȣ������������ٺ�ԭ���������ȣ�
��3�����ɵİ��������С�������������Ȼ�̼�У������Ʒ��ʵ�鷽�����ù��˵õ�����������泥�NH2COONH4����һ�ְ�ɫ���壬�ֽ⣻
��4�����ݷ�Ӧ�����еIJ�����������ܰ���Ⱦ�Ե������ŷŵ������У�����������ˮ��������Ҫ�ŵ�����
��5��̼����淋İ����������Ʒ�У�ʹ̼Ԫ����ȫת��Ϊ̼��ƣ�����̼Ԫ���غ�ͻ���������������ʵ���������
��6������������������Ҫ�ɷ�ΪFe2O3��SiO2��Al2O3 ���Ʊ�FeSO4•7H2O���壬ҪŪ���������ÿһ����ԭ����ע������������м���������ϡ���ᣬFe2O3��Al2O3���������ᷴӦ���ֱ�����Fe2��SO4��2��Al2��SO4��2��SiO2����Ӧ���ȹ��˰�SiO2��ȥ��Ȼ������Һ�м������������ۣ���Fe3+ת����Fe2+�����ݽ������ӳ�����pHֵ��Ȼ��ͨ���μ�NaOH��Һ����pH��5.0��Al3+��ȥ�����ˣ����õ�FeSO4��Һ��Ȼ���������Ũ�������ڱ�ˮ����ȴ����ȴ�ᾧ��֮����ˣ�ϴ�ӣ����º�ɣ�
��� �⣺��1����Ӧ2NH3��g��+CO2��g��?NH2COONH4��s��+Q���Ƿ��ȷ�Ӧ������ƽ��������У��¶����ߣ��������ñ�ˮ��ȴ��߷�Ӧ����ת���ʣ���ֹ�������¶ȹ��߷ֽ⣬
�ʴ�Ϊ�������¶ȣ���߷�Ӧ��ת���ʣ����¶ȣ���ֹ��Ӧ������ɲ���ֽ⣩��
��2��Һ��ʯ������ƿ�������ǿ��Ʒ�Ӧ���г̶ȣ������������ٺ�ԭ���������ȣ�
�ʴ�Ϊ��ͨ���۲����ݣ�����NH3��CO2ͨ�������
��3���Ʊ���������淋�װ����ͼ3��ʾ���Ѱ����Ͷ�����̼ͨ�����Ȼ�̼�У����Ͻ����ϣ����ɵİ��������С�������������Ȼ�̼�У������Ʒ��ʵ�鷽�����ù��˵õ�����������泥�NH2COONH4����һ�ְ�ɫ���壬�ֽ⡢���ܼ��Ⱥ�ɣ�Ӧ�����40�����º�ɣ�
�ʴ𰸣����ˣ�c��
��4��˫ͨ�����ܵ������Ƿ�ֹҺ�嵹����Ũ���������ն���İ�����ͬʱ��ֹ������ˮ�������뷴Ӧ��ʹ���������ˮ�⣬
�ʴ�Ϊ����ֹ���������ն��ఱ������ֹ������ˮ�������뷴Ӧ��ʹ���������ˮ�⣻
��5��ȡ�ֱ��ʶ�����̼����淋İ����������Ʒ0.7820g��������ʯ��ˮ��ִ�����ʹ̼Ԫ����ȫת��Ϊ̼��ƣ����ˡ�ϴ�ӡ�����������Ϊ1.000g�����ʵ���Ϊ0.010mol������Ʒ�а�����������ʵ���Ϊx��̼��������ʵ���Ϊy������̼Ԫ���غ�õ���
x+y=0.01
78x+79y=0.7820
$\left\{\begin{array}{l}{x+y=0.01\\;}\\{78x+79y=0.7820}\end{array}\right.$���$\left\{\begin{array}{l}{x=0.008mol}\\{y=0.002mol}\end{array}\right.$��
����Ʒ�а�������淋����ʵ�������=$\frac{0.008mol}{0.01mol}$��100%=80%��
�ʴ�Ϊ��80%��
��6����������������Ҫ�ɷ�ΪFe2O3��SiO2��Al2O3 ���Ʊ�FeSO4•7H2O���壬�������м���������ϡ���ᣬFe2O3��Al2O3���������ᷴӦ��Fe2O3+3H2SO4�TFe2��SO4��3+3H2O����Al2O3+3H2SO4�TAl2��SO4��3+3H2O���ֱ�����Fe2��SO4��2��Al2��SO4��2��SiO2����Ӧ���ȹ��˰�SiO2��ȥ��Ȼ������Һ�м������������ۣ�2Fe3++Fe�T3Fe2+����Fe3+ת����Fe2+�����ݽ������ӳ�����pHֵ��Ȼ��ͨ���μ�NaOH��Һ����pH��5.0��Al3+��ȥ�����ˣ����õ�FeSO4��Һ���ɼ���Ũ����������Һ��Ȼ����ڱ�ˮ����ȴ����ȴ�ᾧ��֮����ˣ�ϴ�ӣ����º�ɣ�
�ʴ�Ϊ������Һ�м������������ۣ����ˣ���Һ�еμ�NaOH��Һ���ڷ�ӦҺ��pHԼΪ5�����ˣ�
���� ���⿼���������Ʊ�ʵ������Ӧ�ã���Ҫ�ǰ���������Ʊ�ʵ��װ�÷����жϣ�ʵ��������������������ʵ����ƣ��йػ����ļ��㣬��Ŀ�Ѷ��еȣ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | �����£�4���pH=9��Ca��OH��2��Һ��1���pH=13��NaOH��Һ��Ϻ�������Ũ����1��10-13mol/L | |
| B�� | ������ζ���ˮʱ�����÷�̪��ָʾ������̪�ı�ɫ��Χ��pH=8��10�� | |
| C�� | ����Na2CO3��Һ��NaHCO3��Һ��CO2��H2O������Һ�����ǵ�pHֵ�������� | |
| D�� | pH��ͬ�İ�ˮ����������������ˮϡ�͵�ԭ����x����y����pH����ͬ����x��y |
| A�� | �����Ǿ�����ֵ�ߡ�����Ⱦ���ŵ��ȼ�� | |
| B�� | ����ȼ�����ǽ�ˮ��Ϊ�͵�����ȼ�� | |
| C�� | �Ҵ��DZ���������������������ȼ�� | |
| D�� | ʯ�ͺ�ú�ǹ�������ʹ�õĿ������Ļ�ʯȼ�� |
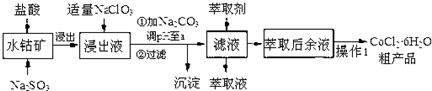
��֪���ٽ���Һ������������Ҫ��H+��Co2+��Fe2+��Mn2+��Al3+�ȣ�
�ڲ��������ӳ���ʱ��Һ��pH���±�������������Ũ��Ϊ��0.01mol/L��
| ������ | Fe��OH��3 | Fe��OH��2 | Co��OH��2 | Al��OH��3 | Mn��OH��2 |
| ��ʼ���� | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| ��ȫ���� | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
��1��д������������Co2O3������Ӧ�����ӷ���ʽCo2O3+SO32-+4H+=2Co2++SO42-+2H2O��
��2��д��������NaClO3������Ӧ����Ҫ���ӷ���ʽClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O��
��3������Na2CO3��pH��a�����������õ��ij���ΪFe��OH��3��Al��OH��3��
��4��������1���а���3������ʵ�������������������Ũ��������ȴ���ᾧ�����ˣ�
��5����ȡ���Խ������ӵ���ȡ����pH�Ĺ�ϵ��ͼ1������Һ���м�����ȡ����Ŀ���dz�ȥ��Һ�е�Mn2+����ʹ�õ����pH��Χ��B����ѡ����ţ���
A��2.0��2.5 B��3.0��3.5 C��4.0��4.5 D��5.0��5.5
��6��Ϊ�ⶨ�ֲ�Ʒ��CoCl2•6H2O��������ȡһ�������Ĵֲ�Ʒ����ˮ����������AgNO3��Һ�����ˡ�ϴ�ӣ���������ɺ����������ͨ�����㷢�ֲִ�Ʒ��CoCl2•6H2O��������������100%����ԭ������Ǵֲ�Ʒ���п������Ȼ������ʧȥ�˲��ֽᾧˮ����һ�����ɣ���
��7����֪ij����ӵ��������LiCoO2����Li+�������Ϊ����ʣ����ʱ��Li+��ԭΪLi������ԭ����ʽǶ
���ظ�������̼-6��C6���У���ͼ2��ʾ�������õ�ص��ܷ�ӦΪLiCoO2+C6$?_{�ŵ�}^{���}$CoO2+LiC6�����طŵ�ʱ��������ӦʽΪ��CoO2+Li++e-=LiCoO2��

| A�� | ���롢�ᴿ��ȷ����ѧʽ��ȷ��ʵ��ʽ��ȷ���ṹʽ | |
| B�� | ���롢�ᴿ��ȷ���ṹʽ��ȷ��ʵ��ʽ��ȷ����ѧʽ | |
| C�� | ���롢�ᴿ��ȷ��ʵ��ʽ��ȷ����ѧʽ��ȷ���ṹʽ | |
| D�� | ȷ����ѧʽ��ȷ��ʵ��ʽ��ȷ���ṹʽ�����롢�ᴿ |
| A�� | �ϳɰ�ʱ�������������������¶ȣ���Ӧ����v��H2����������ƽ��ת���ʾ����� | |
| B�� | 3C��s��+CaO��s��=CaC2��s��+CO��g���ڳ����²����Է����У�˵���÷�Ӧ�ġ�H��0 | |
| C�� | ��ˮ�в���ͨ��CO2������CO2�����ӣ�$\frac{c��O{H}^{-}��}{c��N{H}_{3}•{H}_{2}O��}$�������� | |
| D�� | �������ͭʱ�������Դ������������ͭ���Դ�ĸ������� |