题目内容
沼气是一种能源,它主要是CH4,常温下0.5mol CH4完全燃烧生成CO2和H2O时,放出445kJ的热量,则下列热化学方程式中正确的是( )
| A、2 CH4(g)+4O2(g)=2CO2(g)+4H2O(l);△H=+890kJ/mol |
| B、CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=+890kJ/mol |
| C、CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890kJ/mol |
| D、0.5CH4(g)+O2(g)=0.5CO2(g)+H2O(l);△H=-890kJ/mol |
考点:热化学方程式
专题:
分析:根据热化学方程式的书写方法可知,化学计量数与反应热成正比,并注意标明物质的聚集状态来解答.
解答:
解:0.5mol CH4完全燃烧生成CO2和水时,放出445KJ热量,常温下水为液态,
1molCH4在氧气中燃烧生成CO2和液态水,放出890kJ热量,△H为负值,
则热化学方程式为CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ/mol,
故选C.
1molCH4在氧气中燃烧生成CO2和液态水,放出890kJ热量,△H为负值,
则热化学方程式为CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ/mol,
故选C.
点评:本题主要考查了热化学方程式的书写,难度不大,注意化学计量数与反应热成正比,标明物质的聚集状态.

练习册系列答案
相关题目
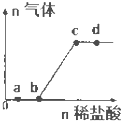 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如右图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如右图所示.则下列离子组在对应的溶液中一定能大量共存的是( )| A、a点对应的溶液中:Na+、OH-、SO42-、NO3- |
| B、b点对应的溶液中:Al3+、Fe3+、NO3-、Cl- |
| C、c点对应的溶液中:Na+、Ca2+、NO3-、Cl- |
| D、d点对应的溶液中:Cl-、NO3-、Fe2+、Na+ |
pH相同的醋酸溶液和盐酸,分别用蒸馏水稀释到原溶液的m倍和n倍,稀释后两溶液的pH仍相同,则m和n的关系量是( )
| A、m=n | B、m>n |
| C、m<n | D、无法判断 |
下列有关实验原理或实验操作正确的是( )


| A、用甲装置验证铜与稀硝酸的反应产物只有NO |
| B、通过乙装置实现化学反应:2Cu+O2+4H+=2Cu2++2H2O |
| C、用适量铜粉除去CuCl2溶液中少量的FeCl3 |
| D、用水湿润的pH试纸测量某溶液的pH |
往下列溶液中滴入FeCl3溶液,不反应的是( )
| A、FeCl2 |
| B、NaOH |
| C、KSCN |
下列说法中,正确的是( )
| A、NH3的水溶液能导电,所以NH3是电解质 |
| B、K2SO4既是钾盐又是硫酸盐 |
| C、向醋酸溶液中加入少量氢氧化钠固体,由于有水生成溶液的导电能力降低 |
| D、稀盐酸能导电所以稀盐酸是电解质 |
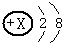 请回答:
请回答: