题目内容
在下列物质中:①NaCl ②NaOH ③Na2O2 ④CO2 ⑤(NH4)2S ⑥CCl4 ⑦C2H2 ⑧SiC ⑨晶体硅 ⑩金刚石(选填序号),含有非极性键的分子晶体是 ;既有离子键,又有极性键和配位键的离子晶体是 ;含有极性键的原子晶体是 .
考点:分子晶体,离子晶体,原子晶体
专题:
分析:同种非金属原子之间形成的化学键为非极性键;
不种非金属原子之间形成的化学键为极性键
离子键为阴阳离子之间形成的化学键;
分子间通过分子间作用力结合形成的晶体为分子晶体;
由阴、阳离子按一定比例通过离子键结合形成的晶体称作离子晶体;
相邻原子之间通过强烈的共价键结合而成的空间网状结构的晶体叫做原子晶体;
根据物质的组成,及有关的概念进行判断.
不种非金属原子之间形成的化学键为极性键
离子键为阴阳离子之间形成的化学键;
分子间通过分子间作用力结合形成的晶体为分子晶体;
由阴、阳离子按一定比例通过离子键结合形成的晶体称作离子晶体;
相邻原子之间通过强烈的共价键结合而成的空间网状结构的晶体叫做原子晶体;
根据物质的组成,及有关的概念进行判断.
解答:
解:①NaCl 只含有离子键;
②NaOH 既有离子键又有共价键,但不存在配位键;
③Na2O2 含有离子键和非极性共价键,属于离子晶体;
④CO2 只存在极性键;
⑤(NH4)2S中阴阳离子之间形成离子键,铵根离子中含有极性共价键和配位键,所以既含有离子键,又含有极性共价键和配位键的离子晶体是(NH4)2S;
⑥CCl4 是由极性共价键形成的非极性分子;
⑦C2H2 中含有的H-C键为极性键,分子间通过分子间作用力结合形成分子晶体;
⑧SiC中C元素与Si元素之间形成极性共价键,相邻原子之间通过强烈的共价键结合而成的空间网状结构属于原子晶体,属于含有极性键的原子晶体的物质;
⑨晶体硅是由非极性键形成的原子晶体;
⑩金刚石是由非极性键形成的原子晶体.
则有非极性键的分子晶体是⑦;既有离子键,又有极性键和配位键的离子晶体是⑤;含有极性键的原子晶体是⑧,
故答案为:⑦;⑤;⑧.
②NaOH 既有离子键又有共价键,但不存在配位键;
③Na2O2 含有离子键和非极性共价键,属于离子晶体;
④CO2 只存在极性键;
⑤(NH4)2S中阴阳离子之间形成离子键,铵根离子中含有极性共价键和配位键,所以既含有离子键,又含有极性共价键和配位键的离子晶体是(NH4)2S;
⑥CCl4 是由极性共价键形成的非极性分子;
⑦C2H2 中含有的H-C键为极性键,分子间通过分子间作用力结合形成分子晶体;
⑧SiC中C元素与Si元素之间形成极性共价键,相邻原子之间通过强烈的共价键结合而成的空间网状结构属于原子晶体,属于含有极性键的原子晶体的物质;
⑨晶体硅是由非极性键形成的原子晶体;
⑩金刚石是由非极性键形成的原子晶体.
则有非极性键的分子晶体是⑦;既有离子键,又有极性键和配位键的离子晶体是⑤;含有极性键的原子晶体是⑧,
故答案为:⑦;⑤;⑧.
点评:本题考查化学键的类型以及晶体的类型,根据物质的组成,及有关的概念进行判断,题目难度不大.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
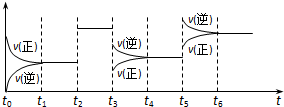
某密闭容器中发生如下反应:X(g)+3Y(g)?2Z(g);△H<0.如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是( )

| A、t5时增大了压强 |
| B、t3时降低了温度 |
| C、t2时加入了催化剂 |
| D、t4~t5时间内转化率一定最低 |
据新浪网报道,欧洲一集团公司拟在太空建立巨大的激光装置,把太阳光变成激光用于分解海水制氢.有下列几种说法:
①水分解反应是放热反应;
②若用生成的氢气与空气中多余的二氧化碳反应生成甲醇储存起来,可改善生存条件;
③使用氢气作燃料有助于控制温室效应;
④氢气是一级能源.
其中叙述正确的是( )
①水分解反应是放热反应;
②若用生成的氢气与空气中多余的二氧化碳反应生成甲醇储存起来,可改善生存条件;
③使用氢气作燃料有助于控制温室效应;
④氢气是一级能源.
其中叙述正确的是( )
| A、①② | B、③④ |
| C、②③ | D、①②③④ |
已知反应A2(g)+2B2(g)?2AB2(g)△H<0,下列说法正确的是( )
| A、升高温度,正向反应速率增加,逆向反应速率减小 |
| B、升高温度有利于反应速率增加,从而缩短达到平衡的时间 |
| C、达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动 |
| D、达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动 |
反应3X(g)+Y(g)?Z(g)+2W(s)在2L密闭容器中进行,5min后Y减少了0.1mol,则此反应的平均速率v为( )
| A、V(X)=0.03mol/(L?min) |
| B、V(Y)=0.02mol/(L?min) |
| C、V(Z)=0.10mol/(L?min) |
| D、V(W)=0.02mol/(L?min) |
沼气是一种能源,它主要是CH4,常温下0.5mol CH4完全燃烧生成CO2和H2O时,放出445kJ的热量,则下列热化学方程式中正确的是( )
| A、2 CH4(g)+4O2(g)=2CO2(g)+4H2O(l);△H=+890kJ/mol |
| B、CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=+890kJ/mol |
| C、CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890kJ/mol |
| D、0.5CH4(g)+O2(g)=0.5CO2(g)+H2O(l);△H=-890kJ/mol |
下列关于铝的说法错误的是( )
| A、铝的表面容易形成致密的氧化膜,抗腐蚀性能好 |
| B、常温下不与任何酸、碱反应 |
| C、铝元素在地壳中的含量高,储量丰富 |
| D、工业上可以用电解法冶炼铝 |
氢化钙可以作为生氢剂(其中CaH2中氢元素为-1价),反应方程式如下:CaH2+2H2O═Ca(OH)2+2H2↑,其中H2是( )
| A、既是氧化产物又是还原产物 |
| B、是氧化剂 |
| C、是还原剂 |
| D、既是氧化剂又是还原剂 |