题目内容
某粒子的结构示意图为: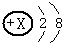 请回答:
请回答:
(1)若该粒子为原子,则X的值为 .
(2)若X的值为11,则该粒子符号为 .
(3)若X的值为 9,那么,X元素与氢元素形成的化合物,电子式为 .
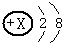 请回答:
请回答:(1)若该粒子为原子,则X的值为
(2)若X的值为11,则该粒子符号为
(3)若X的值为 9,那么,X元素与氢元素形成的化合物,电子式为
考点:原子结构与元素的性质
专题:原子组成与结构专题
分析:原子中核内质子数=核外电子数=原子序数,阴离子中核外电子数=质子数+电荷数,阳离子中核外电子数=质子数-电荷数,据此分析解答.
解答:
解:(1)如果该粒子是原子,原子核外电子数=核内质子数,所以X=2+8=10,故答案为:10;
(2)若X为11,核内质子数>核外电子数,则该粒子是阳离子,电荷数=11-10=1,带一个单位正电荷,为Na+,故答案为:Na+;
(3)若X为9,核内质子数-核外电子数=-1,为阴离子F-,H元素和F元素通过共用电子对形成HF,HF电子式为 ,故答案为:
,故答案为: .
.
(2)若X为11,核内质子数>核外电子数,则该粒子是阳离子,电荷数=11-10=1,带一个单位正电荷,为Na+,故答案为:Na+;
(3)若X为9,核内质子数-核外电子数=-1,为阴离子F-,H元素和F元素通过共用电子对形成HF,HF电子式为
 ,故答案为:
,故答案为: .
.
点评:本题考查原子结构示意图,知道阴阳离子、原子中核外电子数与质子数的关系即可解答,侧重考查学生对基础知识的掌握,注意基础知识的积累,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
沼气是一种能源,它主要是CH4,常温下0.5mol CH4完全燃烧生成CO2和H2O时,放出445kJ的热量,则下列热化学方程式中正确的是( )
| A、2 CH4(g)+4O2(g)=2CO2(g)+4H2O(l);△H=+890kJ/mol |
| B、CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=+890kJ/mol |
| C、CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890kJ/mol |
| D、0.5CH4(g)+O2(g)=0.5CO2(g)+H2O(l);△H=-890kJ/mol |
下列各图所反映的措施中,目的是为了加快其化学反应速率的是( )
A、 铁门表面喷漆 |
B、 冰箱保存食物 |
C、 扇子扇煤炉火 |
D、 |
氢化钙可以作为生氢剂(其中CaH2中氢元素为-1价),反应方程式如下:CaH2+2H2O═Ca(OH)2+2H2↑,其中H2是( )
| A、既是氧化产物又是还原产物 |
| B、是氧化剂 |
| C、是还原剂 |
| D、既是氧化剂又是还原剂 |
有机物的种类繁多,但其命名是有规则的.下列有机物用系统命名法命名正确的是( )
A、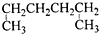 1,4-二甲基丁烷 |
B、 3-甲基丁烯 |
C、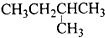 2-甲基丁烷 |
D、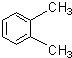 对二甲苯 |
将40℃的饱和石灰水冷却至10℃;或加入少量CaO,但温度仍保持40℃,在这两种情况下均未改变的是( )
| A、Ca(OH)2的溶解度、溶剂的质量 |
| B、溶液中溶质的质量分数 |
| C、溶液的质量、水的电离平衡 |
| D、溶液中Ca2+的数目、溶液中Ca2+的浓度 |
经测定:常温、常压下的一瓶气体中只含有C、O两种元素,通常情况下,这瓶气体不可能是( )
| A、一种纯净的化合物 |
| B、一种单质和一种化合物的混合物 |
| C、两种化合物的混合物 |
| D、两种单质的混合物 |