题目内容
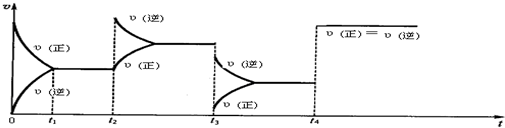
7.在一个恒温、恒容密闭容器中,有两个可左右自由滑动的密封隔板(a、b),将容器分成三部分,已知充入的三种气体质量相等,当隔板静止时,容器内气体所占体积如图所示(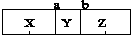 ),下列说法中错误的是( )
),下列说法中错误的是( )| A. | 若Y是C4H8,则X可能是N2 | B. | 分子数目:X=Z=2Y | ||
| C. | 若X是O2,则Z不可能是CO2 | D. | 气体密度:X=Z=2Y |
分析 充入X、Y、Z三种气体,三种气体质量相等,根据ρ=$\frac{m}{V}$知,其密度与体积成反比;当隔板停止滑动时,气体的压强、温度都相等,所以其气体摩尔体积相等,根据V=nVm知,其物质的量之比等于体积之比,据此分析解答.
解答 解:A、设Y的物质的量为1mol,则X为2mol,若Y是C4H8,则X可能是N2,故A正确;
B、分子数目之比等于体积之比,所以分子数目:X=Z=2Y,故B正确;
C、若X是O2,则Z的摩尔质量为:$\frac{1×32}{2}$=16g/mol,所以不可能是CO2,故C正确;
D、根据ρ=$\frac{m}{V}$知,其密度与体积成反比,所以气体密度:2X=2Z=Y,故D错误;故选D.
点评 本题考查阿伏伽德罗定律及其推论,明确相同条件下密度与摩尔质量的关系是解本题关键,正确理解阿伏伽德罗定律及其推论,题目难度中等.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目
17.下列说法正确的是( )
| A. | 常温常压下,11.2 L甲烷气体含有的甲烷分子数为0.5NA | |
| B. | 标准状况下,22.4 L氦气与22.4 L氮气所含原子数相同 | |
| C. | 标准状况下,11.2 L CO与N2的混合气体与11.2 L O2所含分子数相同,原子数也相同 | |
| D. | 标准状况下,22.4 L CCl4中含共价键数为4NA |
18.下列有关物质用途的说法,不正确的是( )
| A. | 制作光纤产品可用晶体硅 | B. | 纸浆漂白可用二氧化硫 | ||
| C. | 游泳池消毒可用漂粉精 | D. | 人工降雨可用干冰 |
15.有机物 的名称为( )
的名称为( )
 的名称为( )
的名称为( )| A. | 3,4-二甲基戊烷 | B. | 1-甲基-2-乙基丁烷 | ||
| C. | 2,3-二甲基戊烷 |
12.下列反应中,不属于四种基本类型反应,但属于氧化还原反应的是( )
| A. | 2CO+O2═2CO2 | B. | CaCO3+2HCl═CaCl2+H2O+CO2↑ | ||
| C. | 2KClO3═2KCl+3O2↑ | D. | Fe2O3+3CO═2Fe+3CO2 |
12.25℃时,在l0mL浓度均为0.1mol.L-1的HC1和CH3COOH混合溶液中滴加0.1mol.L -1NaOH,下列有关溶液中粒子浓度关系正确的是( )
| A. | 未加NaOH时:c(H+)>c(Cl-)=c(CH3COOH) | |
| B. | 加入l0mLNaOH时:c(OH-)+c(CH3COO-)=c(H+) | |
| C. | 加入NaOH至溶液Ph=7时:c(Cl一)-c(Na+) | |
| D. | 加入20mL NaOH时:c(Na+)=c(Cl-)+c(CH3COO一') |