题目内容
19.实验室常利用反应:来制取氯气.MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O(1)用双线桥法标出反应中电子转移的方向和数目.
MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O
(2)该反应中氧化剂是(填化学式,下同)MnO2,氧化产物是Cl2.
(3)该反应中氧化剂与还原剂物质的量之比为1:2.
(4)若有0.5mol MnO2完全反应,则转移的电子的物质的量是1mol.
分析 (1)该反应中Mn元素化合价由+4价变为+2价、Cl元素化合价由-1价变为0价,转移电子数为2;
(2)得电子化合价降低的元素被还原,失电子化合价升高的元素被氧化;
(3)该反应中氧化剂是二氧化锰、有一半的HCl作还原剂;
(4)反应Mn元素化合价由+4价降低到+2价.
解答 解:(1)该反应中Mn元素化合价由+4价变为+2价、Cl元素化合价由-1价变为0价,转移电子数为2,则转移电子方向和数目为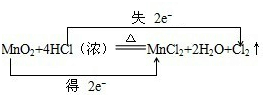 ,故答案为:
,故答案为: ;
;
(2)得电子化合价降低的元素被还原,失电子化合价升高的元素被氧化,该反应中Mn元素化合价由+4价变为+2价、MnO2为氧化剂,Cl元素化合价由-1价变为0价,所以Mn元素被还原、Cl元素被氧化,Cl2为氧化产物,故答案为:MnO2;Cl2;
(3)该反应中氧化剂是二氧化锰、有一半的HCl作还原剂,所以氧化剂和还原剂的物质的量之比为1:2,故答案为:1:2;
(4)反应Mn元素化合价由+4价降低到+2价,则有0.5mol MnO2完全反应,转移的电子的物质的量是1mol,故答案为:1.
点评 本题考查氧化还原反应计算,为高频考点,侧重考查基本概念、基本计算,明确元素化合价变化与概念之间关系是解本题关键,注意:该反应中有一半盐酸作还原剂,一半盐酸体现酸性.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
7.在一个恒温、恒容密闭容器中,有两个可左右自由滑动的密封隔板(a、b),将容器分成三部分,已知充入的三种气体质量相等,当隔板静止时,容器内气体所占体积如图所示( 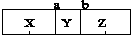 ),下列说法中错误的是( )
),下列说法中错误的是( )
 ),下列说法中错误的是( )
),下列说法中错误的是( )| A. | 若Y是C4H8,则X可能是N2 | B. | 分子数目:X=Z=2Y | ||
| C. | 若X是O2,则Z不可能是CO2 | D. | 气体密度:X=Z=2Y |
14.现有等体积,等物质的量浓度的NaCl、MgCl2、AlCl3三种溶液,用物质的量浓度相同的AgNO3溶液分别完全沉淀三种溶液中的Cl-.所消耗AgNO3溶液的体积比为( )
| A. | 6:3:2 | B. | 3:2:1 | C. | 1:2:3 | D. | 1:1:1 |
4.与50mL 0.1mol/L Na2CO3溶液中Na+的物质的量浓度相同的溶液是( )
| A. | 25 mL 0.2mol/L的NaCl溶液 | B. | 100mL 0.1 mol/L的NaCl溶液 | ||
| C. | 25 mL 0.2 mol/L的Na2SO4溶液 | D. | 10 mL 0.5 mol/L的Na2CO3溶液 |
4.常温下,下列事实能说明亚硝酸是弱电解质的是( )
| A. | NaNO2溶液的pH大于7 | B. | 用HNO2溶液作导电试验,灯泡很暗 | ||
| C. | HNO2不跟NaCl反应 | D. | 可以使石蕊试剂变色 |
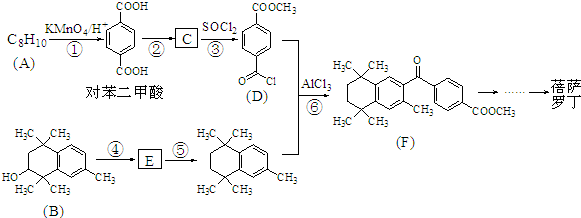
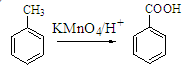 Ⅱ.
Ⅱ.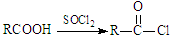
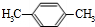 ,C的结构简式为
,C的结构简式为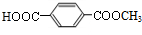 .
. ;⑤
;⑤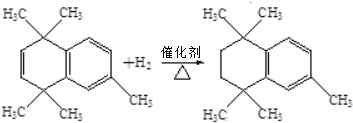 .
.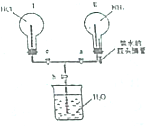 某实验小组在实验室中制取氨气并设计实验验证氨气的某些性质.
某实验小组在实验室中制取氨气并设计实验验证氨气的某些性质.