题目内容
12.下列反应中,不属于四种基本类型反应,但属于氧化还原反应的是( )| A. | 2CO+O2═2CO2 | B. | CaCO3+2HCl═CaCl2+H2O+CO2↑ | ||
| C. | 2KClO3═2KCl+3O2↑ | D. | Fe2O3+3CO═2Fe+3CO2 |
分析 含元素化合价变化的反应为氧化还原反应,四种基本反应类型为化合、分解、置换、复分解,结合物质类别及反应类型来解答.
解答 解:A.为化合反应,C、O元素化合价发生变化,属于氧化还原反应,故A不选;
B.为复分解反应,故B不选;
C.为分解反应,Cl、O元素的化合价变化,为氧化还原反应,故C不选;
D.不属于四种基本反应类型,Fe、C元素的化合价变化,为氧化还原反应,故D选.
故选D.
点评 本题考查氧化还原反应及基本反应类型的判断,为高频考点,把握反应分类及分类依据为解答的关键,注意物质类别及元素化合价判断,题目难度不大.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
2.下列说法正确的是( )
| A. | ${\;}_{22}^{48}$Ti和${\;}_{22}^{50}$Ti的质量数不同,属于两种元素 | |
| B. | ${\;}_{1}^{1}$H2、${\;}_{1}^{2}$H2、H2互为同位素 | |
| C. | 14462Sm其原子核内中子数和质子数都是62 | |
| D. | O2和O3互为同素异形体 |
3.下列各组物质中属于纯净物的是( )
| A. | 氨水 | B. | 氢氧化铁胶体 | C. | 混有冰的水 | D. | 石灰石 |
20.下列说法或表示方法中正确的是( )
| A. | 相同条件下,等质量的硫蒸气和硫固体分别完全燃烧,反应的热效应△H1>△H2 | |
| B. | 由C(石墨)→C(金刚石)△H=+1.9kJ/mol,可知金刚石比石墨稳定 | |
| C. | 已知在101KPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量.则有关氢气燃烧热的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=+285.8kJ/mol | |
| D. | 在稀溶液中,H+ (aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,若将含0.5 mol硫酸的浓硫酸与含1 molNaOH的溶液混合,放出的热量大于57.3 kJ |
7.在一个恒温、恒容密闭容器中,有两个可左右自由滑动的密封隔板(a、b),将容器分成三部分,已知充入的三种气体质量相等,当隔板静止时,容器内气体所占体积如图所示( 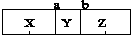 ),下列说法中错误的是( )
),下列说法中错误的是( )
 ),下列说法中错误的是( )
),下列说法中错误的是( )| A. | 若Y是C4H8,则X可能是N2 | B. | 分子数目:X=Z=2Y | ||
| C. | 若X是O2,则Z不可能是CO2 | D. | 气体密度:X=Z=2Y |
4.与50mL 0.1mol/L Na2CO3溶液中Na+的物质的量浓度相同的溶液是( )
| A. | 25 mL 0.2mol/L的NaCl溶液 | B. | 100mL 0.1 mol/L的NaCl溶液 | ||
| C. | 25 mL 0.2 mol/L的Na2SO4溶液 | D. | 10 mL 0.5 mol/L的Na2CO3溶液 |
17.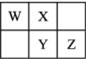 W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )
 W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )| A. | Y元素氧化物对应水化物的酸性一定弱于Z | |
| B. | W、X、Y中最简单氢化物稳定性最强的是X | |
| C. | X元素形成的单核阴离子还原性大于Y | |
| D. | Z元素单质在化学反应中只表现氧化性 |