题目内容
9.将SO2通BaCl2溶液至饱和未见沉淀,继续通入另一种气体仍无沉淀,通入的气体可能是( )| A. | CO2 | B. | NH3 | C. | SO3 | D. | H2S |
分析 将SO2通入BaCl2溶液中 如生成沉淀,应有两种情况,一是溶液中有较多的SO32-离子,或发生氧化还原反应生成SO42-离子.
解答 解:A、SO2与CO2都不与BaCl2反应,并且所对应的酸都比盐酸弱,通入SO2与CO2都不会生成沉淀,故A选;
B、通入NH3溶液呈碱性,溶液中生成大量的SO32-离子,生成沉淀BaSO3,故B不选;
C、SO3与水反应生成SO42-离子,生成沉淀BaSO4,故C不选;
D、H2S与SO2反应生成沉淀S和水,故D不选;
故选A.
点评 本题难度不大,考查SO2的性质,注意SO2的酸性、还原性和氧化性的性质.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案
相关题目
12.2016年全国环境保护工作会议提出要“以改善环境质量为核心,实行最严格的环境保护制度,打好大气、水、土壤污染防治三大战役,确保2020年生态环境质量总体改善”.下列有关环境保护的说法中,正确的是( )
| A. | 纽扣银锌电池体型小,含有害物质少,用后可以随意丢弃 | |
| B. | 化石燃料完全燃烧不会造成大气污染 | |
| C. | “低碳”生活倡导节能减排,应禁止使用化石燃料,减少污水排放 | |
| D. | 将煤气化后再燃烧可减少大气污染 |
20.下列反应能产生Cl2的是( )
| A. | 加热稀盐酸和MnO2的混合物 | |
| B. | 在KMnO4中加入NaCl和浓H2SO4并加热 | |
| C. | KCl加硫酸并加KClO2再加热 | |
| D. | 浓盐酸中加入浓H2SO4并加热 |
17.下列离子组不能在溶液中大量共存并会同时产生沉淀和气体的是( )
| A. | Fe2+、NO3-、K+、Cl- | B. | K+、Al3+、HCO3-、Cl- | ||
| C. | H+、Ca2+、HCO3-、Cl- | D. | Ca2+、HCO3-、OH-、NO3- |
14.请选择适当的试剂,用以除去括号内的杂质,并写出相关的化学方程式
A 氯水 B、Fe C、CO2 D、稀盐酸 E、NaOH溶液 F、氨水
A 氯水 B、Fe C、CO2 D、稀盐酸 E、NaOH溶液 F、氨水
| 物 质 | 加入试剂 | 有关化学方程式 |
| NaHCO3 (Na2CO3)(溶液) | ||
| MgO(Al2O3) |
18.下列叙述正确的是( )
| A. | 通常,同周期元素的第一电离能ⅦA族的元素最大 | |
| B. | 在同一主族中,自上而下第一电离能逐渐减小 | |
| C. | 第ⅠA、ⅡA族元素的原子,其半径越大,第一电离能越大 | |
| D. | 主族元素的原子形成单原子离子时的化合价数都和它的族序数相等 |
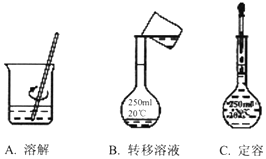 实验室需要配制250mL 1.6mol•L-1的NaOH溶液,请回答下列问题:
实验室需要配制250mL 1.6mol•L-1的NaOH溶液,请回答下列问题: 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.