题目内容
15.下列反应的离子方程式正确的是( )| A. | 向明矾溶液中加入少量的烧碱溶液:Al3++3OH-=Al(OH)3↓ | |
| B. | 在含有等物质的量的Fe(NO3)2和KI组成的混合溶液中滴入稀盐酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O | |
| C. | 碳酸氢铵溶液中滴加少量的NaOH溶液:HCO3-+OH-=CO32-+H2O | |
| D. | 硫化钠溶液呈碱性的原因:S2-+2H2O?H2S+2OH- |
分析 A.氢氧化钠少量,反应生成氢氧化铝沉淀;
B.硝酸根离子在酸性条件下能够氧化碘离子和亚铁离子;
C.氢氧化钠少量,碳酸氢根离子优先反应;
D.硫离子的水解分步进行,离子方程式应该分步书写,主要写出第一步即可.
解答 解:A.向明矾溶液中加入少量的烧碱溶液,反应的离子方程式为:Al3++3OH-=Al(OH)3↓,故A正确;
B.在含有等物质的量的Fe(NO3)2和KI组成的混合溶液中滴入稀盐酸,硝酸根离子在酸性条件下具有强氧化性,能够氧化亚铁离子和碘离子,正确的离子方程式为:6Fe2++6I-+16H++4NO3-=6Fe3++4NO↑+3I2+2H2O,故B错误;
C.碳酸氢铵溶液中滴加少量的NaOH溶液,反应生成碳酸钠、碳酸铵,反应的离子方程式为:HCO3-+OH-=CO32-+H2O,故C正确;
D.硫离子水解生成硫氢根离子和氢氧根离子,则硫化钠溶液呈碱性,反应的离子方程式为:S2-+H2O?HS-+OH-,故D错误;
故选AC.
点评 本题考查了离子方程式的正确判断,为高考的高频题,题目难度中等,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等;试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
5.利用所学化学知识回答问题
Ⅰ、甲醇是重要的化工原料,又可称为燃料.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g)═CH3OH(g)△H=?
②CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=-58kJ/mol
③CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41kJ/mol
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
则x=413kJ/mol.
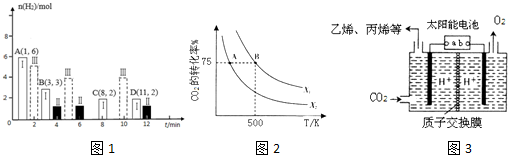
(2)若T℃时将6molCO2和8molH2充入2L密闭容器中发生反应②,测得H2的物质的量随时间变化如图1中状态Ⅰ(图1中实线)所示.图1中数据A(1,6)代表在1min时H2的物质的量是6mol.
①T℃时,状态Ⅰ条件下,平衡常数K=0.5;
②其他条件不变,仅改变温度时,测得H2的物质的量随时间变化如图中状态Ⅲ所示,则状态Ⅲ对应的温度>(填“>”“<”或“=”)T℃;
③一定温度下,此反应在恒容容器中进行,能判断该反应达到化学平衡状态依据的是bc.
a. 2个C=O断裂的同时有2个H-O生成 b.容器中混合气体平均摩尔质量不变
c.v逆(H2)=3v正(CH3OH) d.甲醇和水蒸气的体积比保持不变
Ⅱ、二氧化碳的回收利用是环保领域研究的热点课题.
(1)CO2经过催化氢化合成低碳烯烃.在2L恒容密闭容器中充入2moI CO2和nmol H2,在一定条件下发生反应:2C02(g)+6H2(g)?CH2=CH2(g)+4H20(g),△H=-128kJ/mol.CO2的转化率与温度、投料比[X=$\frac{n({H}_{2})}{n(C{O}_{2})}$]的关系如图2所示.
①X2> X1(填“>”、“<”或“=”)
②在500K时,若B点的投料比为3.5,且从反应开始到B点需要10min,则v(H2)=0.225mol/(L.min).
(2)以稀硫酸为电解质溶液,利用太阳能将CO2转化为低碳烯烃,工作原理图3如下,则左侧产生乙烯的电极反应式为2CO2+12e-+12H+=CH2=CH2+4H2O.

Ⅰ、甲醇是重要的化工原料,又可称为燃料.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g)═CH3OH(g)△H=?
②CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=-58kJ/mol
③CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41kJ/mol
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
| 化学键 | H-H | C-O | C $\frac{\underline{\;←\;}}{\;}$O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 1076 | 465 | x |
(2)若T℃时将6molCO2和8molH2充入2L密闭容器中发生反应②,测得H2的物质的量随时间变化如图1中状态Ⅰ(图1中实线)所示.图1中数据A(1,6)代表在1min时H2的物质的量是6mol.
①T℃时,状态Ⅰ条件下,平衡常数K=0.5;
②其他条件不变,仅改变温度时,测得H2的物质的量随时间变化如图中状态Ⅲ所示,则状态Ⅲ对应的温度>(填“>”“<”或“=”)T℃;
③一定温度下,此反应在恒容容器中进行,能判断该反应达到化学平衡状态依据的是bc.
a. 2个C=O断裂的同时有2个H-O生成 b.容器中混合气体平均摩尔质量不变
c.v逆(H2)=3v正(CH3OH) d.甲醇和水蒸气的体积比保持不变
Ⅱ、二氧化碳的回收利用是环保领域研究的热点课题.
(1)CO2经过催化氢化合成低碳烯烃.在2L恒容密闭容器中充入2moI CO2和nmol H2,在一定条件下发生反应:2C02(g)+6H2(g)?CH2=CH2(g)+4H20(g),△H=-128kJ/mol.CO2的转化率与温度、投料比[X=$\frac{n({H}_{2})}{n(C{O}_{2})}$]的关系如图2所示.
①X2> X1(填“>”、“<”或“=”)
②在500K时,若B点的投料比为3.5,且从反应开始到B点需要10min,则v(H2)=0.225mol/(L.min).
(2)以稀硫酸为电解质溶液,利用太阳能将CO2转化为低碳烯烃,工作原理图3如下,则左侧产生乙烯的电极反应式为2CO2+12e-+12H+=CH2=CH2+4H2O.
6.碳、氮及其化合物在生产中有重要应用.
(1)设反应 ①Fe(s)+CO2(g)?FeO(s)+CO(g)△H=Q1的平衡常数为K1,反应②Fe(s)+H2O(g)?FeO(s)+H2(g)△H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如表:
现有反应 ③H2(g)+CO2(g)?CO(g)+H2O(g)△H=Q3
结合表数据,根据反应①、②推导出推导出Q1、Q2、Q3的关系式Q3=Q1-Q2,反应③是吸热(填“放”或“吸”)热反应.
(2)使用稀土催化剂有效消除汽车尾气中的NOx、碳氢化合物也已逐渐成为成熟技术.压缩天然气汽车利用这一技术将NOx、CH4转化成无毒物质,其中两个反应为:
Ⅰ.CH4(g)+4NO(g)$\frac{\underline{\;催化剂\;}}{\;}$2N2(g)+CO2(g)+2H2O(g)
Ⅱ.CH4(g)+2NO2(g) $\frac{\underline{\;催化剂\;}}{\;}$N2(g)+CO2(g)+2H2O(g)
实验室在恒压下,将CH4(g)和NO2(g)置于密闭容器中发生反应Ⅱ,测得在不同温度、不同投料比时,NO2的平衡转化率如表:
①写出该反应平衡常数的表达式K=$\frac{c({N}_{2})•c(C{O}_{2})•{c}^{2}({H}_{2}O)}{c(C{H}_{4})•{c}^{2}(N{O}_{2})}$,若降低温度,提高[n(NO2)/n(CH4)]
投料比,则K将增大.(填“增大”、“减小”或“不变”)
②400K时,将投料比为1的NO2和CH4的混合气体共0.04mol,充入一装有催化剂的容器中,充分反应后,平衡时NO2的体积分数17.4%.
③收集某汽车尾气经测量NOx的含量为1.12%(体积分数),若用甲烷将其完全转化为无害气体,处理1×104L(标准状况下)该尾气需要甲烷30g,则尾气中V(NO):V(NO2)=1:1.
④在密闭容器内先通入一定量的CH4,然后再充入一定量的NO2.在不同温度下,同时发生反应Ⅱ:并在 t秒时测定其中NO2转化率,绘得图象如图所示:
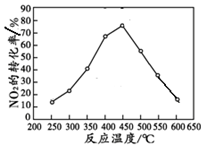
产生这一现象的原因是在250℃-450℃时,NOx转化率随温度升高而增大:反应未建立平衡,温度升高反应正向进行.450℃-600℃(温度较高)时,反应已达平衡,所以,温度升高平衡逆向移动,NOx转化率随温度升高反而减小.
(1)设反应 ①Fe(s)+CO2(g)?FeO(s)+CO(g)△H=Q1的平衡常数为K1,反应②Fe(s)+H2O(g)?FeO(s)+H2(g)△H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如表:
| T/K | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
结合表数据,根据反应①、②推导出推导出Q1、Q2、Q3的关系式Q3=Q1-Q2,反应③是吸热(填“放”或“吸”)热反应.
(2)使用稀土催化剂有效消除汽车尾气中的NOx、碳氢化合物也已逐渐成为成熟技术.压缩天然气汽车利用这一技术将NOx、CH4转化成无毒物质,其中两个反应为:
Ⅰ.CH4(g)+4NO(g)$\frac{\underline{\;催化剂\;}}{\;}$2N2(g)+CO2(g)+2H2O(g)
Ⅱ.CH4(g)+2NO2(g) $\frac{\underline{\;催化剂\;}}{\;}$N2(g)+CO2(g)+2H2O(g)
实验室在恒压下,将CH4(g)和NO2(g)置于密闭容器中发生反应Ⅱ,测得在不同温度、不同投料比时,NO2的平衡转化率如表:
| 投料比[n(NO2)/n(CH4)] | 400 K | 500 K | 600 K |
| 1 | 60% | 43% | 28% |
| 2 | 45% | 33% | 20% |
投料比,则K将增大.(填“增大”、“减小”或“不变”)
②400K时,将投料比为1的NO2和CH4的混合气体共0.04mol,充入一装有催化剂的容器中,充分反应后,平衡时NO2的体积分数17.4%.
③收集某汽车尾气经测量NOx的含量为1.12%(体积分数),若用甲烷将其完全转化为无害气体,处理1×104L(标准状况下)该尾气需要甲烷30g,则尾气中V(NO):V(NO2)=1:1.
④在密闭容器内先通入一定量的CH4,然后再充入一定量的NO2.在不同温度下,同时发生反应Ⅱ:并在 t秒时测定其中NO2转化率,绘得图象如图所示:

产生这一现象的原因是在250℃-450℃时,NOx转化率随温度升高而增大:反应未建立平衡,温度升高反应正向进行.450℃-600℃(温度较高)时,反应已达平衡,所以,温度升高平衡逆向移动,NOx转化率随温度升高反而减小.
3.下列热化学方程式或说法正确的是( )
| A. | 甲烷的燃烧热为△H=-890kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890 kJ?mol-1 | |
| B. | 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | 已知:H2(g)+F2(g)=2HF(g);△H=-270 kJ/mol,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 KJ | |
| D. | 在C中相同条件下,2 mol HF气体的能量小于1 mol氢气与1 mol氟气的能量总和 |
20.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | c(Fe3+)=0.1 mol•L-1的溶液中:K+、ClO-、SO42-、SCN- | |
| B. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:NH4+、Al3+、NO3-、Cl- | |
| C. | 由水电离产生的c(OH-)=1×10-13mol/L的溶液中:Ca2+、K+、Cl-、HCO3- | |
| D. | pH=1的溶液中:Fe2+、NO3-、SO42-、Na+ |
7. 向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以如表和如图表示:
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以如表和如图表示:
下列说法正确的是( )
 向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以如表和如图表示:
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以如表和如图表示:| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5 L | 0.5 L | 1.0 L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物 起始量 | 1.5 mol A 0.5 mol B | 1.5 mol A 0.5 mol B | 6.0 mol A 2.0 mol B |
| A. | 平衡后,向甲容器中再充入0.5 mol A,A和B的转化率均增大 | |
| B. | 达到平衡时反应吸收的热量:Q丙>2Q乙 | |
| C. | 若平衡时保持温度不变,改变容器体积平衡不移动 | |
| D. | T1℃,起始时甲容器中充入0.5 mol A、1.5 mol B,平衡时A的转化率为25% |
4.恒容容器中,2SO2(g)+O2(g)?2SO3 (g)△H=-296.6kJ/mol,下列判断不正确的是( )
| A. | 2体积SO2和足量O2反应,一定不能生成2体积SO3 | |
| B. | 其他条件不变,增大压强,正反应速率增大逆反应速率也增大 | |
| C. | 加入2molSO2和1molO2放出的热量是加入1molSO2和0.5molO2放出热量的2倍 | |
| D. | 在该容器中先投入1molSO3,平衡后再加入1molSO3,达新平衡后SO2的体积分数比原平衡减小 |
5.下列说法正确的是( )
| A. | 增大反应物的浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大 | |
| B. | 有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 | |
| C. | 升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数 | |
| D. | 催化剂虽然不参加化学反应,但能增大单位体积内活化分子的数目,从而增大反应速率 |