题目内容
6.碳、氮及其化合物在生产中有重要应用.(1)设反应 ①Fe(s)+CO2(g)?FeO(s)+CO(g)△H=Q1的平衡常数为K1,反应②Fe(s)+H2O(g)?FeO(s)+H2(g)△H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如表:
| T/K | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
结合表数据,根据反应①、②推导出推导出Q1、Q2、Q3的关系式Q3=Q1-Q2,反应③是吸热(填“放”或“吸”)热反应.
(2)使用稀土催化剂有效消除汽车尾气中的NOx、碳氢化合物也已逐渐成为成熟技术.压缩天然气汽车利用这一技术将NOx、CH4转化成无毒物质,其中两个反应为:
Ⅰ.CH4(g)+4NO(g)$\frac{\underline{\;催化剂\;}}{\;}$2N2(g)+CO2(g)+2H2O(g)
Ⅱ.CH4(g)+2NO2(g) $\frac{\underline{\;催化剂\;}}{\;}$N2(g)+CO2(g)+2H2O(g)
实验室在恒压下,将CH4(g)和NO2(g)置于密闭容器中发生反应Ⅱ,测得在不同温度、不同投料比时,NO2的平衡转化率如表:
| 投料比[n(NO2)/n(CH4)] | 400 K | 500 K | 600 K |
| 1 | 60% | 43% | 28% |
| 2 | 45% | 33% | 20% |
投料比,则K将增大.(填“增大”、“减小”或“不变”)
②400K时,将投料比为1的NO2和CH4的混合气体共0.04mol,充入一装有催化剂的容器中,充分反应后,平衡时NO2的体积分数17.4%.
③收集某汽车尾气经测量NOx的含量为1.12%(体积分数),若用甲烷将其完全转化为无害气体,处理1×104L(标准状况下)该尾气需要甲烷30g,则尾气中V(NO):V(NO2)=1:1.
④在密闭容器内先通入一定量的CH4,然后再充入一定量的NO2.在不同温度下,同时发生反应Ⅱ:并在 t秒时测定其中NO2转化率,绘得图象如图所示:
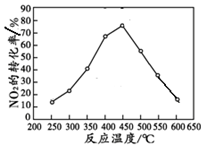
产生这一现象的原因是在250℃-450℃时,NOx转化率随温度升高而增大:反应未建立平衡,温度升高反应正向进行.450℃-600℃(温度较高)时,反应已达平衡,所以,温度升高平衡逆向移动,NOx转化率随温度升高反而减小.
分析 (1)已知:①Fe(s)+CO2(g)?FeO(s)+CO(g)△H=Q1
②Fe(s)+H2O(g)?FeO(s)+H2(g)△H=Q2
由盖斯定律①-②得③H2(g)+CO2(g)?CO(g)+H2O(g)计算Q3,结合图表中平衡常数随温度变化分析反应热量变化;
(2)①根据化学平衡常数为生成物浓度幂之积与反应物浓度幂之积之比列式;反应Ⅱ为放热反应,降低温度,化学平衡常数增大;
②400K时,将投料比为1的NO2和CH4的混合气体共0.04mol,则NO2和CH4的各0.02mol,二氧化氮转化率为60%,依据化学平衡三段式列式计算;
③依据一氧化氮、二氧化氮变化为氮气,甲烷变化为二氧化碳过程中电子转移守恒列式计算;
④在250℃-450℃时,NOx转化率随温度升高而增大:反应未建立平衡,温度升高反应正向进行. 450℃-600℃(温度较高)时,反应已达平衡,所以,温度升高平衡逆向移动,NOx转化率随温度升高反而减小.
解答 解:(1)由图可知反应 ①的K1随温度升高而增大,说明正反应为吸热反应,△H>0,反应 ②的K2随温度升高而减小,说明正反应为放热反应,△H<0,
已知:①Fe(s)+CO2(g)?FeO(s)+CO(g)△H=Q1>0
②Fe(s)+H2O(g)?FeO(s)+H2(g)△H=Q2<0
由盖斯定律①-②得③H2(g)+CO2(g)?CO(g)+H2O(g))△H=Q3=Q1-Q2>0,说明是个吸热反应;
故答案为:Q1-Q2;吸热;
(2)①Ⅱ、CH4(g)+2NO2(g) $\frac{\underline{\;催化剂\;}}{\;}$N2(g)+CO2(g)+2H2O(g)
则化学平衡常数K=$\frac{c({N}_{2})•{c}^{2}({H}_{2}O)•c(C{O}_{2})}{c(C{H}_{4})•{c}^{2}(N{O}_{2})}$;反应Ⅱ为放热反应,降低温度,化学平衡常数增大;
故答案为:$\frac{c({N}_{2})•{c}^{2}({H}_{2}O)•c(C{O}_{2})}{c(C{H}_{4})•{c}^{2}(N{O}_{2})}$;增大;
②400K时,将投料比为1的NO2和CH4的混合气体共0.04mol,则NO2和CH4的各0.02mol,二氧化氮转化率为60%,则
CH4(g)+2NO2(g)$\frac{\underline{\;催化剂\;}}{\;}$N2(g)+CO2(g)+2H2O(g)
n始 0.02 0.02 0 0 0
n转 0.006 0.02×0.6=0.012 0.006 0.006 0.012
n平 0.014 0.008 0.006 0.006 0.012
平衡时NO2的体积分数为:$\frac{0.008}{0.014+0.008+0.006+0.006+0.012}×100%$=17.4%;
故答案为:17.4%;
③收集某汽车尾气经测量NOx的含量为1.12%(体积分数),若用甲烷将其完全转化为无害气体,处理1×104L(标准状况下)该尾气的物质的量为:1.12%×1×104L÷22.4L/mol=5mol,需要甲烷30g,设尾气中NO物质的量为x,NO2物质的量为y,2NO~N2~4e-,2NO2~N2~4e-,CH4~CO2~8e-,
2x+4y=$\frac{30g}{16g/L}×8$=15,
x+y=5,解得x=2.5mol,y=2.5mol,尾气中V(NO):V(NO2)=1:1;
故答案为:1:1;
④在250℃-450℃时,NOx转化率随温度升高而增大:反应未建立平衡,温度升高反应正向进行. 450℃-600℃(温度较高)时,反应已达平衡,所以,温度升高平衡逆向移动,NOx转化率随温度升高反而减小;
故答案为:在250℃-450℃时,NOx转化率随温度升高而增大:反应未建立平衡,温度升高反应正向进行. 450℃-600℃(温度较高)时,反应已达平衡,所以,温度升高平衡逆向移动,NOx转化率随温度升高反而减小.
点评 本题考查化学平衡常数计算及影响因素、平衡状态判断、盖斯定律应用等,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不变化说明到达平衡,注意图象变化规律的理解应用,掌握平衡移动原理是关键,题目难度较大.

 期末集结号系列答案
期末集结号系列答案| A. | 加入水时,平衡向逆反应方向移动 | |
| B. | 加入少量CH3COONa固体,平衡向逆反应方向移动,c(CH3COO-)增大 | |
| C. | 加入少量0.1 mol•L-1HCl溶液,平衡向逆反应方向移动,溶液中c(H+)减小 | |
| D. | 加入少量NaOH固体,平衡向正反应方向移动,酸性增强 |
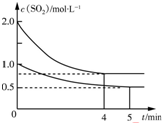 向甲、乙两个容积均为1L的恒温恒容的密闭容器中,分别充入一定量的SO2和O2(其中,甲充入2mol SO2、1mol O2,乙充入1mol SO2、0.5mol O2),发生反应:2SO2(g)+O2(g)?2SO3(g)△H=-197.74kJ•mol-1.一段时间后达到平衡,测得两容器中c(SO2)(mol•L-1)随时间t(min)的变化关系如图所示.下列说法正确的是( )
向甲、乙两个容积均为1L的恒温恒容的密闭容器中,分别充入一定量的SO2和O2(其中,甲充入2mol SO2、1mol O2,乙充入1mol SO2、0.5mol O2),发生反应:2SO2(g)+O2(g)?2SO3(g)△H=-197.74kJ•mol-1.一段时间后达到平衡,测得两容器中c(SO2)(mol•L-1)随时间t(min)的变化关系如图所示.下列说法正确的是( )| A. | 放出的热量Q:Q(甲)>2Q(乙) | |
| B. | 体系总压强p:p(甲)>2p(乙) | |
| C. | 乙中前5 min内的反应速率v(O2)=0.05mol•L-1•min-1 | |
| D. | 保持其他条件不变,若起始时向乙中充入0.4 mol SO2、0.2 mol O2、0.4 mol SO3,则此时v(正)>v(逆) |
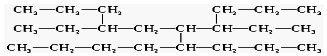
命名该有机物时,应认定它的主链上的碳原子数目是( )
| A. | 8 | B. | 9 | C. | 11 | D. | 12 |
| A. | Fe(OH)2 | B. | A l(OH)3 | C. | Fe(OH)3 | D. | Al(OH)3 和Fe(OH)3 |
| A. | 向明矾溶液中加入少量的烧碱溶液:Al3++3OH-=Al(OH)3↓ | |
| B. | 在含有等物质的量的Fe(NO3)2和KI组成的混合溶液中滴入稀盐酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O | |
| C. | 碳酸氢铵溶液中滴加少量的NaOH溶液:HCO3-+OH-=CO32-+H2O | |
| D. | 硫化钠溶液呈碱性的原因:S2-+2H2O?H2S+2OH- |
| A. | 将AlCl3溶液和Al2(SO4)3溶液分别加热、蒸干、灼烧,所得固体成分相同 | |
| B. | 配制FeSO4溶液时,将FeSO4固体溶于稀盐酸中,然后稀释至所需浓度 | |
| C. | 用带磨口玻璃塞的试剂瓶保存Na2CO3溶液 | |
| D. | 洗涤油污常用热的碳酸钠溶液 |

