题目内容
12.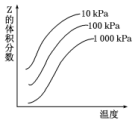 如图是温度和压强对反应X+Y?2Z影响的示意图.图中纵坐标表示平衡混合气体中Z的体积分数.下列叙述正确的是( )
如图是温度和压强对反应X+Y?2Z影响的示意图.图中纵坐标表示平衡混合气体中Z的体积分数.下列叙述正确的是( )| A. | 恒容时,混合气体的密度可作为此反应是否达到化学平衡状态的判断依据 | |
| B. | X、Y、Z均为气态 | |
| C. | 上述反应的逆反应的△H>0 | |
| D. | 使用催化剂Z的产率提高 |
分析 由图可知,温度越高,Z的体积分数越大,升高温度平衡正向移动,可知正反应为△H>0;温度相同时压强越大,Z的体积分数越小,则增大压强平衡逆向移动,X、Y中只有一种为气体,以此来解答.
解答 解:A.由上述分析可知,X、Y中只有一种为气体,则混合气体的质量为变量,可知密度为变量,则恒容时,混合气体的密度可作为此反应是否达到化学平衡状态的判断依据,故A正确;
B.由上述分析可知,X、Y中只有一种为气体,故B错误;
C.正反应为△H>0,则逆反应为△H<0,故C错误;
D.催化剂对平衡移动无影响,则使用催化剂Z的产率不变,故D错误;
故选A.
点评 本题考查化学平衡,为高频考点,把握图中温度、压强对平衡移动的影响为解答该题的关键,侧重分析与应用能力的考查,注意选项A为解答的易错点,题目难度不大.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
3.反应N2+3H2?2NH3,在2L的密闭容器内进行到半分钟时,有0.6mol NH3生成,则下列反应速率不正确的是( )
| A. | ${V}_{N{H}_{3}}$=0.6mol/L•min | B. | ${V}_{{N}_{2}}$=0.005mol/L•s | ||
| C. | ${V}_{{H}_{2}}$=0.9mol/L•min | D. | ${V}_{N{H}_{3}}$=0.02mol/L•s |
20.不锈钢是由铁、铬、镍,碳及众多不同元素所组成的合金,铁是主要成分元素,铬是笫一主要的合金元素.其中铬的含量不能低于11%,不然就不能生成致密氧化膜CrO3以防止腐蚀.

(1)基态碳(C)原子的电甲排布图为 .
.
(2)[Cr(H20)4Cl2]•2H2O 中Cr的配位数为6.
(3)与铜属于同一周期,且未成对电子数最多的元素基态原子价层电子排布式为3d54s1.
(4)Fe的一种晶胞结构如甲、乙所示,若按甲中虚线方向切乙得到的A〜D图中正确的是A.
(5)据报道,只含镁、镍和碳三种元素的晶体具 有超导性.鉴于这三种元素都是常见元素,从而引起广泛关注.该晶体的晶胞结构如下图所示,晶体中每个镁原子周围距离最近的镍原子有12个,试写出该晶体的化学式MgCNi3.
(6)根据下列五种元素的第一至第四电离能数据(单位:kJ•mol-1),回答下列问题.
①在周期表中,最可能处于同一族的是R和U.
②T元素最可能是P区元素.若T为第二周期元素,F.是第三周期元素中原子半径最小的元素,则T、F形成的化合物的空间构型为平面三角形,其中心原子的杂化方式为sp2.

(1)基态碳(C)原子的电甲排布图为
 .
.(2)[Cr(H20)4Cl2]•2H2O 中Cr的配位数为6.
(3)与铜属于同一周期,且未成对电子数最多的元素基态原子价层电子排布式为3d54s1.
(4)Fe的一种晶胞结构如甲、乙所示,若按甲中虚线方向切乙得到的A〜D图中正确的是A.
(5)据报道,只含镁、镍和碳三种元素的晶体具 有超导性.鉴于这三种元素都是常见元素,从而引起广泛关注.该晶体的晶胞结构如下图所示,晶体中每个镁原子周围距离最近的镍原子有12个,试写出该晶体的化学式MgCNi3.
(6)根据下列五种元素的第一至第四电离能数据(单位:kJ•mol-1),回答下列问题.
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2 080 | 4 000 | 6 100 | 9 400 |
| R | 500 | 4 600 | 6 900 | 9 500 |
| S | 740 | 1 500 | 7 700 | 10 500 |
| T | 580 | 1 800 | 2 700 | 11 600 |
| U | 420 | 3 100 | 4 400 | 5 900 |
②T元素最可能是P区元素.若T为第二周期元素,F.是第三周期元素中原子半径最小的元素,则T、F形成的化合物的空间构型为平面三角形,其中心原子的杂化方式为sp2.
7.化合物的分离和提纯是物质制备过程中的重要步骤,下列混合物选择的分离试剂和提纯方法均正确的是( )
| 选项 | 目的 | 除杂试剂 | 实验方法 |
| A | 除去CuCO3固体中的(NH4)2CO3 | - | 置于坩埚中加热至恒重 |
| B | 除去Ag2S中少量AgCl | Na2S溶液 | 过滤 |
| C | 除去乙稀中的SO2气体 | 酸性高锰酸钾溶液 | 洗气 |
| D | 除去甘油中的乙酸 | NaOH溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
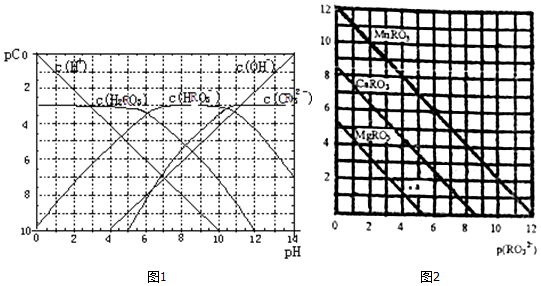
17.25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)CH3COOH、H2CO3、HC1O的酸性由强到弱的顺序为CH3COOH>H2CO3>HC1O.
(2)写出H2CO3的电离方程式:H2CO3?HCO3-+H+,HCO3-?CO32-+H+.
(3)常温下0.1mol•L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是A(填宇母序号,下同).
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$
C.c(H+)•c(OH-) D.$\frac{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}{c(C{H}_{3}COOH)}$
若该溶液升髙温度,上述4种表达式的数据增大的是ABCD.
(4)取0.10mol CH3COOH (冰醋酸)作导电性实验,测得其导电率随加入的水量变化如图所示:比较a、b点的相关性质(填“>”“<”或“=”):
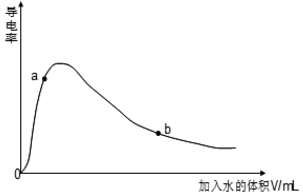
n(H+):a<b;c(CH3COO-):a>b;完全中和时消耗NaOH的物质的量:a=b;
(5)H+浓度相同等体积的两份溶液A(盐酸)和B(CH3COOH)分別与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是③④(填写序号)
①反应所需要的时间B>A ②开始反应时的速率A>B
③参加反应的锌的物质的量A=B ④A中有锌剩余.
| 化学式 | CH3COOH | H2CO3 | HC1O |
| 电离平衡常数 | 1.7×10-5 | K1=4.3×10 K2=5.6×10-11 | 3.0×10-8 |
(1)CH3COOH、H2CO3、HC1O的酸性由强到弱的顺序为CH3COOH>H2CO3>HC1O.
(2)写出H2CO3的电离方程式:H2CO3?HCO3-+H+,HCO3-?CO32-+H+.
(3)常温下0.1mol•L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是A(填宇母序号,下同).
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$
C.c(H+)•c(OH-) D.$\frac{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}{c(C{H}_{3}COOH)}$
若该溶液升髙温度,上述4种表达式的数据增大的是ABCD.
(4)取0.10mol CH3COOH (冰醋酸)作导电性实验,测得其导电率随加入的水量变化如图所示:比较a、b点的相关性质(填“>”“<”或“=”):

n(H+):a<b;c(CH3COO-):a>b;完全中和时消耗NaOH的物质的量:a=b;
(5)H+浓度相同等体积的两份溶液A(盐酸)和B(CH3COOH)分別与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是③④(填写序号)
①反应所需要的时间B>A ②开始反应时的速率A>B
③参加反应的锌的物质的量A=B ④A中有锌剩余.
2. 化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.
化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.
Ⅰ.测定化学反应速率
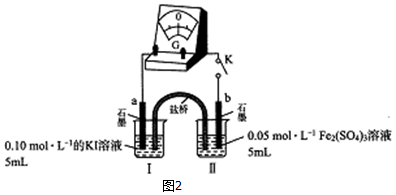
该同学利用如图装置测定化学反应速率.
(已知:S2O32-+2H+=H2O+S↓+SO2↑)
(1)为保证实验准确性、可靠性,利用该装置进行实验前应先进行的步骤是检查装置的气密性;除如图所示的实验用品、仪器外,还需要的一件实验仪器是秒表.
(2)若在2min时收集到224mL(已折算成标准状况)气体,可计算出该2min内H+的反应速率,而该测定值比实际值偏小,其原因是SO2会部分溶于水,导致所测得SO2体积偏小.
(3)试简述测定该反应的化学反应速率的其他方法(写一种):测定一段时间内生成硫单质的质量或测定一定时间内溶液H+浓度的变化
Ⅱ.为探讨化学反应速率的影响因素,设计的实验方案如下表.
(已知 I2+2S2O32-=S4O62-+2I-,其中Na2S2O3溶液均足量)
(4)该实验进行的目的是探究反应物浓度(Na2S2O3)对化学反应速率的影响;,表中Vx=4 mL,比较t1、t2、t3大小,试推测该实验结论:t1<t2<t3.
 化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.
化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.Ⅰ.测定化学反应速率
该同学利用如图装置测定化学反应速率.
(已知:S2O32-+2H+=H2O+S↓+SO2↑)
(1)为保证实验准确性、可靠性,利用该装置进行实验前应先进行的步骤是检查装置的气密性;除如图所示的实验用品、仪器外,还需要的一件实验仪器是秒表.
(2)若在2min时收集到224mL(已折算成标准状况)气体,可计算出该2min内H+的反应速率,而该测定值比实际值偏小,其原因是SO2会部分溶于水,导致所测得SO2体积偏小.
(3)试简述测定该反应的化学反应速率的其他方法(写一种):测定一段时间内生成硫单质的质量或测定一定时间内溶液H+浓度的变化
Ⅱ.为探讨化学反应速率的影响因素,设计的实验方案如下表.
(已知 I2+2S2O32-=S4O62-+2I-,其中Na2S2O3溶液均足量)
| 实验序号 | 体积V/mL | 时间/s | |||
| Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
| ① | 10.0 | 2.0 | 4.0 | 0.0 | t1 |
| ② | 8.0 | 2.0 | 4.0 | 2.0 | t2 |
| ③ | 6.0 | 2.0 | 4.0 | Vx | t3 |