题目内容
14.污水经过一级、二级处理后,还含有少量Cu2+、Hg2+、Pb2+等重金属离子,可加入沉淀剂使其沉淀.下列物质不能作为沉淀剂的是( )A.氨水 B.硫化氢气体 C.硫酸钠溶液 D.双氧水.
分析 各项所加试剂均应过量才符合题目要求,A项溶液形成络离子,B项生成硫化铜、硫化汞、硫化铅等沉淀,C项硫酸铜不是沉淀,D项均能通过双水解调节pH转化为沉淀.
解答 解:A.加入氨水,易形成络离子,不能生成沉淀,故A错误;
B.加入硫化氢气体,生成硫化铜、硫化汞、硫化铅等沉淀,故B正确;
C.不能使Cu2+生成沉淀,故C错误;
D.均能通过双氧水解调节pH转化为沉淀,故D正确.
故选AC.
点评 本题考查离子反应的条件,离子反应的实质学生容易接受,比较基础.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
4.通过该反应可制得ClO2:2KClO3+H2C2O4+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2ClO2↑+K2SO4+2CO2↑+2H2O,下列说法不正确的是( )
| A. | H2C2O4在反应中作还原剂 | |
| B. | 该反应中氧化产物与还原产物的物质的量之比为1:1 | |
| C. | KClO3在反应中得到电子 | |
| D. | 1 molKClO3参加反应有2mol电子转移 |
9.下列实验操作或记录正确的是( )
| A. | 用盐酸滴定氢氧化钠溶液时向锥形瓶中量取25.00mL的氢氧化钠溶液 | |
| B. | 用量筒测得排水法收集制得的氢气体积为50.28 mL | |
| C. | 用两只250 mL的容量瓶配制0.1 mol•L-1 500 mL的NaOH溶液 | |
| D. | 用托盘天平称取2.50 g胆矾,受热充分失水后,固体质量减轻0.90 g |
4.下列物质碱性最强的是( )
| A. | LiOH | B. | KOH | C. | RbOH | D. | NaOH |
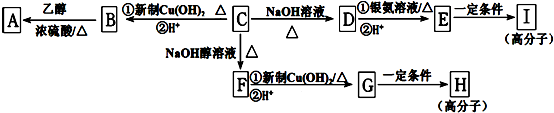
 ;
;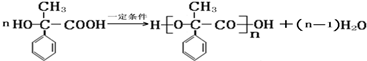 ,该反应类型是缩聚反应;
,该反应类型是缩聚反应; ,该反应类型是加聚反应;
,该反应类型是加聚反应; .
.