题目内容
19.各种必需元素在人体内的含量都有一个最佳范围,过高或过低都有可能影响人正常的生理机能.在日常生活中应注意合理的摄取人体必需的元素.(1)蛋白质是构成生命的基础物质,使日常膳食的重要组成部分.下列食物中富含蛋白质的是③.
①苹果 ②葡萄干 ③牛奶 ④白菜
(2)当人体缺少碘元素或碘元素含量过高时,都会引起甲状腺疾病.由于我国居民每天摄入的碘元素不足,因此我国政府从1994年起推出全民食用加碘盐工程,目前“加碘盐”主要是在实验中加入碘酸钾,碘酸钾的化学式为KIO3.
分析 (1)肉类、乳制品富含蛋白质;
(2)碘酸钾的化学式为KIO3.
解答 解:(1)苹果白菜富含维生素;葡萄干富含糖类;牛奶富含蛋白质,故答案为:③;
(2)碘酸钾的化学式为KIO3,故答案为:KIO3.
点评 本题考查氨基酸、蛋白质的结构和性质特点和化学式的书写,难度不大,掌握各种营养素的生理功能、食物来源等是正确解题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.能正确表示下列反应的离子方程式的是( )
| A. | 等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-═Mg(OH)2↓ | |
| B. | 向Fe(NO3)3溶液中通入足量HI气体:2Fe3++2I-═2Fe2++I2 | |
| C. | 向NaHCO3溶液中滴入少量澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| D. | 向水玻璃溶液中通入过量CO2:SiO32-+H2O+CO2═CO32-+H2SiO3↓ |
7.下列有关除杂质(括号中为杂质)的操作中,错误的是( )
| A. | 福尔马林(蚁酸):加入足量饱和碳酸钠溶液充分振荡,蒸馏,收集馏出物 | |
| B. | 甘油(水):用分液漏斗分离 | |
| C. | 苯(苯酚):加NaOH溶液,充分振荡,分液 | |
| D. | 乙酸乙酯(乙酸):加饱和碳酸钠溶液,充分振荡,分液 |
4.在水溶液中能大量共存的一组离子是( )
| A. | CO32-、H+、NO3-、Na+ | B. | OH-、K+、NO3-、Cl- | ||
| C. | Mg2+、H+、OH-、SO42- | D. | Na+、Cu2+、OH-、SO42- |
8.设NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 一定条件下,6.4 g铜与过量的硫反应,转移电子数目为0.2NA | |
| B. | 3mol单质Fe完全转变为Fe3O4,失去8NA个电子 | |
| C. | 标准状况下,11.2L SO3 中含有2NA个原子 | |
| D. | 用石灰乳完全吸收1 mol Cl2时,转移电子的数目是2NA |
9.下列气体属于无色、无味、有毒的气体是( )
| A. | CO | B. | SO2 | C. | CO2 | D. | H2S |
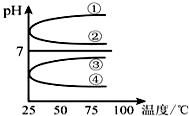 (1)稀释0.1mol•L-1氨水时,随着水量的增加而减小的是①②(填写序号).
(1)稀释0.1mol•L-1氨水时,随着水量的增加而减小的是①②(填写序号).