题目内容
8.相同状况下,1.12L乙烷和丁烷的混合物完全燃烧需O2 4.76L,则混合气中乙烷的体积分数是( )| A. | 25% | B. | 35% | C. | 65% | D. | 75% |
分析 发生C2H6+$\frac{7}{2}$O2$\stackrel{点燃}{→}$2CO2+3H2O、C4H10+$\frac{13}{2}$O2$\stackrel{点燃}{→}$4CO2+5H2O,结合体积之比等于物质的量之比计算.
解答 解:发生C2H6+$\frac{7}{2}$O2$\stackrel{点燃}{→}$2CO2+3H2O、C4H10+$\frac{13}{2}$O2$\stackrel{点燃}{→}$4CO2+5H2O,
设混合气中乙烷为xL,丁烷为yL,则
$\left\{\begin{array}{l}{x+y=1.12}\\{3.5x+6.5y=4.76}\end{array}\right.$
解得x=0.84L,
可知混合气中乙烷的体积分数是$\frac{0.84L}{1.12L}$×100%=75%,
故选D.
点评 本题考查有机反应的计算,为高频考点,把握发生的燃烧反应及体积关系为解答的关键,侧重分析与推断能力的考查,注意体积与物质的量关系,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.下列实验“操作和现象”与“结论”对应关系正确的是( )
| A. | 向盛有某溶液的试管中加入盐酸酸化的硝酸钡,产生白色沉淀,则该溶液中一定含SO42- | |
| B. | 向盛有某溶液的试管中加入浓的强碱溶液,加热,用润湿的蓝色石蕊试纸置于管口,试纸变红,则该溶液中一定含有NH4+ | |
| C. | 向盛有某溶液的试管中加入硝酸银溶液,产生了白色沉淀,则该溶液中一定含有Cl- | |
| D. | 向盛有某溶液的试管中加入加入KSCN溶液显红色.则该溶液中一定含有Fe3+ |
19.化学与科学、技术、社会、环境密切相关,下列有关说法中错误的是( )
| A. | 2010 年 11 月广州亚运会燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 | |
| B. | 合金的硬度一般比它的各成分金属的小,多数合金的熔点一般也比它的各成分金属 的高 | |
| C. | 小苏打是制作馒头和面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂 | |
| D. | 青铜是我国使用最早的合金材料,目前世界上使用量最大的合金材料是钢铁 |
16. 25℃时,三种酸的电离平衡常数如表所示.
25℃时,三种酸的电离平衡常数如表所示.
回答下列问题:
(1)亚磷酸(H3PO3) 为二元中强酸,具有较强的还原性,可将银离子还原成银单质,在空气可缓慢氧化成H3PO4.H3PO3的电离方程式为H3PO3?H2PO3-+H+(H2PO3-?HPO32-+H+).
(2)物质的量浓度均为0.1mol•L-1的三种溶液:a.CH3COONa b.NaClO c.NaHPO3
它们的pH由小到大排列顺序是b>c>a(用字母表示).
(3)常温下,0.1mol•L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是A(填字母).
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
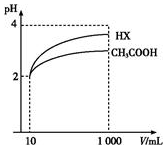
(4)体积为10mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的平衡常数.
 25℃时,三种酸的电离平衡常数如表所示.
25℃时,三种酸的电离平衡常数如表所示.| 化学式 | CH3COOH | HClO | H3PO3 |
| 名称 | 醋酸 | 次氯酸 | 亚磷酸 |
| 电离平衡常数(25℃) | 1.8×10-5 | 3.0×10-8 | K1=8.3×10-3 K2=5.6×10-6 |
(1)亚磷酸(H3PO3) 为二元中强酸,具有较强的还原性,可将银离子还原成银单质,在空气可缓慢氧化成H3PO4.H3PO3的电离方程式为H3PO3?H2PO3-+H+(H2PO3-?HPO32-+H+).
(2)物质的量浓度均为0.1mol•L-1的三种溶液:a.CH3COONa b.NaClO c.NaHPO3
它们的pH由小到大排列顺序是b>c>a(用字母表示).
(3)常温下,0.1mol•L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是A(填字母).
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(4)体积为10mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的平衡常数.
3.在Na2CO3溶液中,下列等量关系成立的是( )
| A. | c(OH-)=c(HCO3-)+c(H2CO3) | B. | 2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | ||
| C. | c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) | D. | c(Na+)>c(CO32-)>c(OH-)>c(HCO3-) |
13.取三个干燥的烧瓶,分别装入标准状况下的干燥氨气、含有二分之一体积空气的氯化氢、二氧化氮和氧气(体积比为4:1)的混合气体;然后分别做溶解于水的喷泉实验.实验结束后三个烧瓶中所得溶液的物质的量浓度之比为( )
| A. | 2:1:2 | B. | 1:1:1 | C. | 5:5:4 | D. | 7:7:4 |
20.实验室中药品的保存有一定的要求.下列做法不正确的是( )
| A. | 液溴需用少量水液封 | |
| B. | NaOH固体最好盛放在塑料瓶中 | |
| C. | FeSO4溶液需加入少量硫酸和铁粉 | |
| D. | 浓硝酸用带橡胶塞的棕色细口瓶盛放 |
17.X、Y、Z、W、Q五种短周期元素在元素周期表中的位置如表所示,其中X元素原子的最外层电子数是最内层电子数的3倍,则下列说法一定正确的是( )
| X | Y | |
| Z | W | Q |
| A. | X、W能分别与钠形成摩尔质量相同且阴、阳离子个数比为1:2的化合物 | |
| B. | X和Z只能形成一种化合物 | |
| C. | 氧化物对应的水化物酸性:W<Q | |
| D. | 原子半径大小关系:Q>W>Z>Y |