题目内容
17.氯化钠、氢氧化钠、碳酸钠和碳酸氢钠是生活中常见的物质.请回答下列问题.(1)等质量的碳酸钠和碳酸氢钠与足量盐酸反应时生成CO2的量,前者<后者(填>、<或=).
(2)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为HCO3-+H+=CO2↑+H2O.
(3)除去NaHCO3溶液中的少量Na2CO3,方法是:通入足量的CO2,离子方程式:CO32-+CO2+H2O=2HCO3-.
分析 (1)等质量的碳酸钠和碳酸氢钠,由$\frac{m}{106}$<$\frac{m}{84}$可知,碳酸氢钠的物质的量大,结合碳原子守恒分析;
(2)碳酸氢钠与盐酸反应生成氯化钠、水、二氧化碳;
(3)碳酸钠、水、二氧化碳反应生成碳酸氢钠.
解答 解:(1)等质量的碳酸钠和碳酸氢钠,由$\frac{m}{106}$<$\frac{m}{84}$可知,碳酸氢钠的物质的量大,由碳原子守恒可知,生成CO2的量前者<后者,故答案为:<;
(2)碳酸氢钠与盐酸反应生成氯化钠、水、二氧化碳,离子反应为HCO3-+H+=CO2↑+H2O,故答案为:HCO3-+H+=CO2↑+H2O;
(3)除去NaHCO3溶液中的少量Na2CO3,方法是通入足量的CO2,发生的离子反应为CO32-+CO2+H2O=2HCO3-,
故答案为:通入足量的CO2;CO32-+CO2+H2O=2HCO3-.
点评 本题考查离子反应方程式的书写及混合物分离提纯,为高频考点,把握物质的性质、发生的反应及离子反应的书写为解答的关键,侧重分析与应用能力的考查,注意钠的化合物的性质及转化,题目难度不大.

练习册系列答案
相关题目
7.下列贮存化学试剂的方法正确的是( )
| A. | 新制的氯水保存在棕色广口瓶中,并放在阴凉处 | |
| B. | 波尔多液(CuSO4与石灰水按一定比例混合)盛放在铁制容器中 | |
| C. | 烧碱溶液放在带玻璃塞的磨口试剂瓶中 | |
| D. | 金属钠保存在煤油中 |
8.在指定环境中,下列各组离子可以大量共存的是( )
| A. | 加入铝片立即放出氢气的溶液中:C1-、K+、NH4+、NO3- | |
| B. | 滴加石蕊试液呈红色的溶液中:CO32-、K+、ClO-、OH- | |
| C. | pH=13的溶液中:HCO3-、Na+、NO3-、SO42 | |
| D. | 在pH=3的溶液中:NH4+、Ca2+、C1-、K+ |
5.室温条件下进行如表各组实验,其中的观察要点不能说明醋酸是弱电解质的是( )
| 选项 | 实验方案 | 观察要点 |
| A | 等浓度的醋酸与氢氧化钠溶液反应 | 恰好反应时的体积比 |
| B | 醋酸溶液中加入醋酸钠固体 | 溶液pH的变化 |
| C | 等体积等浓度的盐酸和醋酸分别和等量镁条反应 | 产生H2的起始速率 |
| D | 将pH=4的醋酸稀释成PH=6的溶液 | 加H2O的量 |
| A. | A | B. | B | C. | C | D. | D |
12.芳香化合物M的结构简式为  关于有机物M的说法正确的是( )
关于有机物M的说法正确的是( )
 关于有机物M的说法正确的是( )
关于有机物M的说法正确的是( )| A. | 有机物M的分子式为C10H12O3 | |
| B. | 1 mol Na2CO3最多能消耗1 mol有机物M | |
| C. | 1 mol M和足量金属钠反应生成22.4 L气体 | |
| D. | 有机物M能发生取代、氧化、还原和加聚反应 |
3.下列粒子结构示意图中,表示Mg2+的是( )
| A. | 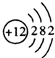 | B. | 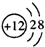 | C. | 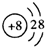 | D. | 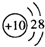 |
 (1)已知反应:H2+Cl2$→_{400℃}^{CuO/CuCl_{2}}$2HCl,已知H-H键能为436kJ/mol,Cl-Cl键能为243kJ/mol,H-Cl键能为432kJ/mol.
(1)已知反应:H2+Cl2$→_{400℃}^{CuO/CuCl_{2}}$2HCl,已知H-H键能为436kJ/mol,Cl-Cl键能为243kJ/mol,H-Cl键能为432kJ/mol.