��Ŀ����
��֪2RCH2CHO
 ˮ������EΪ���������ռ������������Ʒ�ɹ˪��E��һ�ֺϳ�·�����£�
ˮ������EΪ���������ռ������������Ʒ�ɹ˪��E��һ�ֺϳ�·�����£�

��ش��������⣺
��1������һԪ��A��������������ԼΪ21.6%����A�ķ���ʽΪ ���ṹ������ʾAֻ��һ������A������Ϊ ��
��2��B�ܷ���������Ӧ���÷�Ӧ�Ļ�ѧ����ʽΪ ��
��3��C�� �ֹ����ţ���һ��ȡ��������C�����������ţ���ʹ�õ��Ⱥ�˳��д�������Լ� ��
��4���ڢ۲��ķ�Ӧ����Ϊ ��D���������ŵ�����Ϊ ��
��5��д��ͬʱ��������������ˮ�����ͬ���칹��Ľṹ��ʽ������дһ�֣� ��
a�������к���6��̼ԭ����һ�����ϣ�
b�����������������Ű���ˮ������еĹ�����
��6��д��E�Ľṹ��ʽ ��
| NaOH/H2O |
| �� |
 ˮ������EΪ���������ռ������������Ʒ�ɹ˪��E��һ�ֺϳ�·�����£�
ˮ������EΪ���������ռ������������Ʒ�ɹ˪��E��һ�ֺϳ�·�����£�
��ش��������⣺
��1������һԪ��A��������������ԼΪ21.6%����A�ķ���ʽΪ
��2��B�ܷ���������Ӧ���÷�Ӧ�Ļ�ѧ����ʽΪ
��3��C��
��4���ڢ۲��ķ�Ӧ����Ϊ
��5��д��ͬʱ��������������ˮ�����ͬ���칹��Ľṹ��ʽ������дһ�֣�
a�������к���6��̼ԭ����һ�����ϣ�
b�����������������Ű���ˮ������еĹ�����
��6��д��E�Ľṹ��ʽ
���㣺�л�����ƶ�
ר�⣺�л���Ļ�ѧ���ʼ��ƶ�
����������һԪ��A��������������ԼΪ21.6%�����һԪ����ͨʽΪCnH2n+2O����Ԫ�ص���������=
��100%=21.6%��n=4����A�ķ���ʽΪC4H10O���ṹ������ʾAֻ��һ��������A�Ľṹ��ʽΪCH3CH2CH2CH2OH��A��Cu�����������������±���������B��B�ܷ���������Ӧ����B�ṹ��ʽΪCH3CH2CH2CHO��1-��ȩ��NaOH/H2O�����·����ӳ�����C��C�ṹ��ʽΪCH3CH2CH2CH=C��CH2CH3��CHO��C��Ӧ����D��EΪˮ������������ͼ��ת����ϵ֪��D�к��д��ǻ�����D��Է�������Ϊ130����D�ṹ��ʽΪCH3CH2CH2CH2CH��CH2CH3��CH2OH��C�����������ӳɷ�Ӧ����D��D�����ǻ������ᷢ��������Ӧ����E��E�ṹ��ʽΪ ���ݴ˷������
���ݴ˷������
| 16 |
| 16+14n+2 |
 ���ݴ˷������
���ݴ˷���������
�⣺һԪ��A��������������ԼΪ21.6%�����һԪ����ͨʽΪCnH2n+2O����Ԫ�ص���������=
��100%=21.6%��n=4����A�ķ���ʽΪC4H10O���ṹ������ʾAֻ��һ��������A�Ľṹ��ʽΪCH3CH2CH2CH2OH��A��Cu�����������������±���������B��B�ܷ���������Ӧ����B�ṹ��ʽΪCH3CH2CH2CHO��1-��ȩ��NaOH/H2O�����·����ӳ�����C��C�ṹ��ʽΪCH3CH2CH2CH=C��CH2CH3��CHO��C��Ӧ����D��EΪˮ������������ͼ��ת����ϵ֪��D�к��д��ǻ�����D��Է�������Ϊ130����D�ṹ��ʽΪCH3CH2CH2CH2CH��CH2CH3��CH2OH��C�����������ӳɷ�Ӧ����D��D�����ǻ������ᷢ��������Ӧ����E��E�ṹ��ʽΪ ��
��
��1��ͨ�����Ϸ���֪��A�ķ���ʽΪC4H10O��A������Ϊ1-�������ʴ�Ϊ��C4H10O��1-������
��2��B�ṹ��ʽΪCH3CH2CH2CHO��B��������Һ����������Ӧ���÷�Ӧ�Ļ�ѧ����ʽΪCH3CH2CH2CHO+2[Ag��NH3��2]OH
CH3CH2CH2COONH4+2Ag��+3NH3+H2O���ʴ�Ϊ��CH3CH2CH2CHO+2[Ag��NH3��2]OH
CH3CH2CH2COONH4+2Ag��+3NH3+H2O��
��3��C�ṹ��ʽΪCH3CH2CH2CH=C��CH2CH3��CHO��C��̼̼˫����ȩ�����ֹ����ţ�����̼̼˫������ˮ������ȩ����������Һ�������ܺ�̼̼˫������������Ӧ��������ȩ��������Ҫ�ȼ���ȩ�������̼̼˫��������һ��ȡ��������C�����������ţ���ʹ�õ��Ⱥ�˳��д�������Լ�Ϊ������Һ��ϡ���ᡢ��ˮ��
�ʴ�Ϊ��2��������Һ��ϡ���ᡢ��ˮ��
��4���ڢ۲�ΪC�����������ӳɷ�Ӧ����D�����Ը÷�Ӧ�ķ�Ӧ����Ϊ�ӳɷ�Ӧ��D�ṹ��ʽΪCH3CH2CH2CH2CH��CH2CH3��CH2OH��D���������ŵ�����Ϊ�ǻ����ʴ�Ϊ���ӳɷ�Ӧ���ǻ���
��5��ˮ����IJ����Ͷ���5��������Ŀ����������֪ˮ�����ͬ���칹����뺬��һ���Ȼ���һ���ǻ�������������ֵ�̼̼���������������Ľṹ��ʽΪ�� ��
��
 ��
�� ��
�� ������4�ֹʴ�Ϊ��
������4�ֹʴ�Ϊ�� ��
��
 ��
�� ��
�� ����дһ�֣���
����дһ�֣���
��6��ͨ�����Ϸ���֪��E�Ľṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
| 16 |
| 16+14n+2 |
 ��
����1��ͨ�����Ϸ���֪��A�ķ���ʽΪC4H10O��A������Ϊ1-�������ʴ�Ϊ��C4H10O��1-������
��2��B�ṹ��ʽΪCH3CH2CH2CHO��B��������Һ����������Ӧ���÷�Ӧ�Ļ�ѧ����ʽΪCH3CH2CH2CHO+2[Ag��NH3��2]OH
| �� |
| �� |
��3��C�ṹ��ʽΪCH3CH2CH2CH=C��CH2CH3��CHO��C��̼̼˫����ȩ�����ֹ����ţ�����̼̼˫������ˮ������ȩ����������Һ�������ܺ�̼̼˫������������Ӧ��������ȩ��������Ҫ�ȼ���ȩ�������̼̼˫��������һ��ȡ��������C�����������ţ���ʹ�õ��Ⱥ�˳��д�������Լ�Ϊ������Һ��ϡ���ᡢ��ˮ��
�ʴ�Ϊ��2��������Һ��ϡ���ᡢ��ˮ��
��4���ڢ۲�ΪC�����������ӳɷ�Ӧ����D�����Ը÷�Ӧ�ķ�Ӧ����Ϊ�ӳɷ�Ӧ��D�ṹ��ʽΪCH3CH2CH2CH2CH��CH2CH3��CH2OH��D���������ŵ�����Ϊ�ǻ����ʴ�Ϊ���ӳɷ�Ӧ���ǻ���
��5��ˮ����IJ����Ͷ���5��������Ŀ����������֪ˮ�����ͬ���칹����뺬��һ���Ȼ���һ���ǻ�������������ֵ�̼̼���������������Ľṹ��ʽΪ��
 ��
�� ��
�� ��
�� ������4�ֹʴ�Ϊ��
������4�ֹʴ�Ϊ�� ��
�� ��
�� ��
�� ����дһ�֣���
����дһ�֣�����6��ͨ�����Ϸ���֪��E�Ľṹ��ʽΪ
 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
���������⿼���л����ƶϣ����ؿ���������ƶ���������ȷ�ƶ�A�ṹ�ǽⱾ��ؼ���ע�������Ϣ������ȩ���ӷ�Ӧʱ�ϼ��ͳɼ���ʽ��ע�⣨3���й����ż���˳����Щ�����״��㣮

��ϰ��ϵ�д�
 ������ϵ�д�
������ϵ�д�
�����Ŀ
NAΪ�����ӵ�������������������ȷ���У�������
| A��1molFeCl3��ȫת��������������������� NA������ |
| B��1molH2O2��MnO2������ú�ת��2NA������ |
| C����״���£�22.4��H2��4�˺�������NA������ |
| D��50�棬1��105Pa��46��NO2��0�棬2��105Pa��46��N2O4������3NA��ԭ�� |
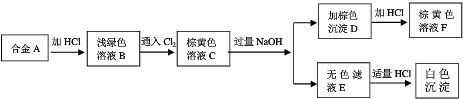
��������ɫ��Һ�У����Դ���������������ǣ�������
| A��K+��Na+��Cl-��CO32- |
| B��Cu2+��Cl-��Na+��SO42- |
| C��Ca2+��Na+��Cl-��NO3- |
| D��Fe3+��NH4+��SCN-��HCO3-�� |
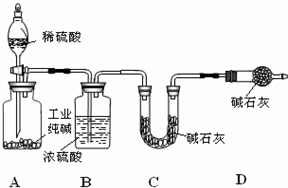 ��ҵ�����г�����NaCl��Na2SO4���ʣ�Ϊ�˲ⶨ��ҵ������Na2CO3�ĺ�����ijͬѧ�������ͼװ�ã�
��ҵ�����г�����NaCl��Na2SO4���ʣ�Ϊ�˲ⶨ��ҵ������Na2CO3�ĺ�����ijͬѧ�������ͼװ�ã�
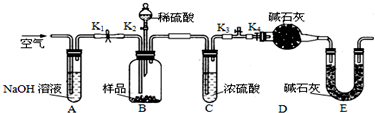
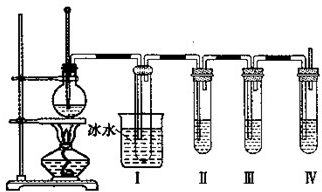 ʵ������ȡ��ϩ��������ϩ����ʵ���װ����ͼ��ʾ����ش�
ʵ������ȡ��ϩ��������ϩ����ʵ���װ����ͼ��ʾ����ش�