题目内容
NA为阿伏加德罗常数,下列叙述中正确的有( )
| A、1molFeCl3完全转化成氢氧化铁胶体后生成 NA个胶粒 |
| B、1molH2O2与MnO2充分作用后,转移2NA个电子 |
| C、标准状况下,22.4升H2与4克氦气均含NA个分子 |
| D、50℃,1×105Pa下46克NO2与0℃,2×105Pa下46克N2O4均含有3NA个原子 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、氢氧化铁胶粒为氢氧化铁的聚集体,无法计算氢氧化铁胶粒的数目;
B、H2O2与MnO2作用时,MnO2做催化剂,H2O2发生歧化反应;
C、气体体积换算物质的量,质量换算物质的量,氦气是单原子分子;
D、46gNO2的物质的量不受温度和压强的影响.
B、H2O2与MnO2作用时,MnO2做催化剂,H2O2发生歧化反应;
C、气体体积换算物质的量,质量换算物质的量,氦气是单原子分子;
D、46gNO2的物质的量不受温度和压强的影响.
解答:
解:A.氢氧化铁胶粒为氢氧化铁的聚集体,1mol铁离子形成的氢氧化铁胶粒的物质的量一定小于1mol,故A错误;
B、H2O2与MnO2作用时,MnO2做催化剂,H2O2发生歧化反应,1molH2O2转移1mol电子,故B错误;
C、标准状况下22.4L氢气物质的量为1mol,4g氦气物质的量为1mol,故含有的分子个数相同,故C正确;
D、46gNO2的物质的量不受温度和压强的影响,46克NO2的物质的量n=
=
=1mol,含有3mol原子,故D正确.
故选CD.
B、H2O2与MnO2作用时,MnO2做催化剂,H2O2发生歧化反应,1molH2O2转移1mol电子,故B错误;
C、标准状况下22.4L氢气物质的量为1mol,4g氦气物质的量为1mol,故含有的分子个数相同,故C正确;
D、46gNO2的物质的量不受温度和压强的影响,46克NO2的物质的量n=
| m |
| M |
| 46g |
| 46g/mol |
故选CD.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
将一块银白色的金属钠放在空气中会发生一系列的变化:表面迅速变暗→“出汗”→变成白色固体粉末.下列有关叙述不正确的是( )
| A、表面迅速变暗是因为生成了氧化钠 |
| B、“出汗”是因为表面形成了NaOH溶液 |
| C、白色固体粉末是碳酸钠 |
| D、以上三个过程均发生了氧化还原反应 |
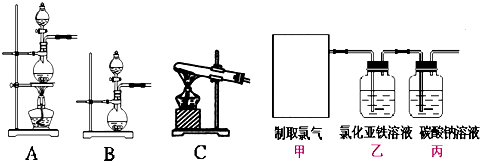
根据原电池形成的条件分析图所示的各装置,其中有电流通过的是( )
A、 乙醇 |
B、 稀硫酸 |
C、 |
D、 稀硫酸 |
下列叙述一定正确的是( )
| A、H2O、D2O、T2O互为同位素 |
| B、pH=1的溶液中,K+、Na+、NO3-、S2O32-不能大量共存 |
| C、元素周期表中从上至下同主族元素的氢化物的熔、沸点依次升高 |
| D、乙炔、氢气、铁分别与氯气反应,都会因用量或条件不同而生成不同产物 |
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA |
| B、标准状况下,22.4L己烷中共价键数目为19NA |
| C、由SO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
| D、1L浓度为1mol?L-1的Na2CO3溶液中含有NA个CO32- |
表示下列变化的化学用语正确的是( )
| A、NaHCO3的水解:HCO3-+H2O?H3O++CO32- | ||||
| B、1L 0.5mol?L-1稀硫酸与1L 1mol?L-1氢氧化钠溶液反应放出57.3kJ的热量:H2SO4(aq)+2NaOH(aq)═Na2SO4(aq)+2H2O(1);△H=-57.3 kJ/mol | ||||
| C、氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH- | ||||
D、以惰性电极电解KCl溶液:2Cl-+2H2O
|
 水杨酸酯E为紫外线吸收剂,可用于配制防晒霜.E的一种合成路线如下:
水杨酸酯E为紫外线吸收剂,可用于配制防晒霜.E的一种合成路线如下: