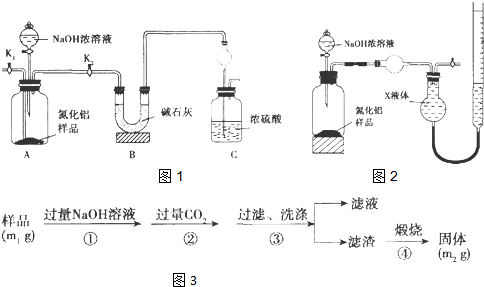
题目内容
某校化学兴趣小组将一定浓度NaHCO3溶液加入到CuSO4溶液中发现生成了蓝绿色颗粒状沉淀.他们对此产生了浓厚的兴趣,查阅了相关资料之后,结合元素守恒,他们提出了如下三种假设:
假设一:沉淀是 ;
假设二:沉淀是Cu(OH)2
假设三:沉淀是CuCO3和Cu(OH)2的混合物
(1)请写出有Cu(OH)2生成的理由 (用离子方程式表示);
(2)为了探究沉淀的成分,他们取出了一部分沉淀,滴加稀盐酸,发现有气体放出.凭此现象,他们判断沉淀中含有 ;于是,得出假设 不成立.
(3)为了进一步探究沉淀的成份,进而确定剩余两种假设中何种假设成立,他们设计实验,装置图如下:
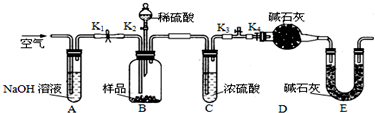
①在研究沉淀物组成前,须将沉淀从溶液中分离并净化.具体操作依次为 、洗涤、干燥;
②装置E中碱石灰的作用是 ;
③实验过程中有以下操作步骤:a.打开K1、K3,关闭K2、K4,通入过量空气. b.关闭K1、K3,打开K2、K4充分反应 c.打开K1、K4,关闭K2、K3,通入过量空气.步骤a的作用是 ;
④已知沉淀样品的质量为m g,装置D的质量增加了n g,若沉淀样品为纯净物,m、n之间的关系为,若假设三成立,CuCO3的质量分数为;若不进行步骤C,则会使测得结果 (填“偏高”“无影响”“偏低”)
假设一:沉淀是
假设二:沉淀是Cu(OH)2
假设三:沉淀是CuCO3和Cu(OH)2的混合物
(1)请写出有Cu(OH)2生成的理由
(2)为了探究沉淀的成分,他们取出了一部分沉淀,滴加稀盐酸,发现有气体放出.凭此现象,他们判断沉淀中含有
(3)为了进一步探究沉淀的成份,进而确定剩余两种假设中何种假设成立,他们设计实验,装置图如下:

①在研究沉淀物组成前,须将沉淀从溶液中分离并净化.具体操作依次为
②装置E中碱石灰的作用是
③实验过程中有以下操作步骤:a.打开K1、K3,关闭K2、K4,通入过量空气. b.关闭K1、K3,打开K2、K4充分反应 c.打开K1、K4,关闭K2、K3,通入过量空气.步骤a的作用是
④已知沉淀样品的质量为m g,装置D的质量增加了n g,若沉淀样品为纯净物,m、n之间的关系为,若假设三成立,CuCO3的质量分数为;若不进行步骤C,则会使测得结果
考点:探究物质的组成或测量物质的含量
专题:
分析:根据逻辑分析,可知假设一的内容.
(1)假设二沉淀为氢氧化铜的判断依据是碳酸氢钠和硫酸铜在水溶液中发生双水解生成分析;
(2)取出了一部分沉淀,滴加稀盐酸,有气体放出,证明沉淀中含有碳酸铜;
(3)①将沉淀从溶液中分离并净化的实验步骤为过滤、洗涤、干燥;
②装置E中装有碱石灰,防止空气中的二氧化碳和水蒸气进入装置D,造成测定误差;
③空气中含有二氧化碳,空气通过氢氧化钠溶液吸收空气中的二氧化碳,利用除去二氧化碳的空气,打开K1、K3,关闭K2、K4,排除装置中的含二氧化碳气体的空气,避免测定误差的产生;
④若沉淀样品的质量为m g,若沉淀样品为纯净物,则判断沉淀为CuCO3,装置D的质量增加了n g,为二氧化碳气体质量,依据碳元素守恒得到mn的关系;若假设三正确,依据生成的二氧化碳物质的量减少碳酸铜质量,根据样品质量计算得到氢氧化铜的质量分数.
(1)假设二沉淀为氢氧化铜的判断依据是碳酸氢钠和硫酸铜在水溶液中发生双水解生成分析;
(2)取出了一部分沉淀,滴加稀盐酸,有气体放出,证明沉淀中含有碳酸铜;
(3)①将沉淀从溶液中分离并净化的实验步骤为过滤、洗涤、干燥;
②装置E中装有碱石灰,防止空气中的二氧化碳和水蒸气进入装置D,造成测定误差;
③空气中含有二氧化碳,空气通过氢氧化钠溶液吸收空气中的二氧化碳,利用除去二氧化碳的空气,打开K1、K3,关闭K2、K4,排除装置中的含二氧化碳气体的空气,避免测定误差的产生;
④若沉淀样品的质量为m g,若沉淀样品为纯净物,则判断沉淀为CuCO3,装置D的质量增加了n g,为二氧化碳气体质量,依据碳元素守恒得到mn的关系;若假设三正确,依据生成的二氧化碳物质的量减少碳酸铜质量,根据样品质量计算得到氢氧化铜的质量分数.
解答:
解:根据逻辑分析,又假设二、三,可知假设一:沉淀是CuCO3.
(1)假设2沉淀为氢氧化铜的判断依据是碳酸氢钠和硫酸铜在水溶液中发生双水解生成,反应的离子方程式为Cu2++2HCO3-=Cu (OH)2↓+2CO2↑,
故答案为:Cu2++2HCO3-=Cu (OH)2↓+2CO2↑;
(2)取出了一部分沉淀,滴加稀盐酸,有气体放出,依据沉淀的组成可能是碳酸铜,则假设二不成立,故答案为:碳酸铜、二;
(3)①分析题干可知,将沉淀从溶液中分离并净化的实验步骤为过滤、洗涤、干燥,故答案为:过滤;
②装装置E中装有碱石灰,防止空气中的二氧化碳和水蒸气进入装置D,造成测定误差,故答案为:防止空气中的水蒸气和CO2被D吸收影响CO2质量的测定;
③空气中含有二氧化碳,空气通过氢氧化钠溶液吸收空气中的二氧化碳,利用除去二氧化碳的空气,打开K1、K3,关闭K2、K4,排除装置中的含二氧化碳气体的空气,避免测定误差的产生;
故答案为:排尽装置中空气中的CO2使测定结果准确;
④若沉淀样品的质量为m g,若沉淀样品为纯净物,则判断沉淀为CuCO3,装置D的质量增加了n g,为二氧化碳气体质量,依据碳元素守恒得到mg=
mol×124g/mol,得到mn的关系为31n=11m;若假设三正确,依据生成的二氧化碳物质的量减少碳酸铜质量,根据样品质量计算得到氢氧化铜的质量分数=
×100%=
×100%,若不进行步骤C,生成的二氧化碳气体中含有水蒸气,被装置D吸收后称量得到二氧化碳质量增大,计算得到碳酸铜质量增大,氢氧化铜的质量减小,则会使测得结果质量分数偏低,
故答案为:31n=11m;
×100%;偏低.
(1)假设2沉淀为氢氧化铜的判断依据是碳酸氢钠和硫酸铜在水溶液中发生双水解生成,反应的离子方程式为Cu2++2HCO3-=Cu (OH)2↓+2CO2↑,
故答案为:Cu2++2HCO3-=Cu (OH)2↓+2CO2↑;
(2)取出了一部分沉淀,滴加稀盐酸,有气体放出,依据沉淀的组成可能是碳酸铜,则假设二不成立,故答案为:碳酸铜、二;
(3)①分析题干可知,将沉淀从溶液中分离并净化的实验步骤为过滤、洗涤、干燥,故答案为:过滤;
②装装置E中装有碱石灰,防止空气中的二氧化碳和水蒸气进入装置D,造成测定误差,故答案为:防止空气中的水蒸气和CO2被D吸收影响CO2质量的测定;
③空气中含有二氧化碳,空气通过氢氧化钠溶液吸收空气中的二氧化碳,利用除去二氧化碳的空气,打开K1、K3,关闭K2、K4,排除装置中的含二氧化碳气体的空气,避免测定误差的产生;
故答案为:排尽装置中空气中的CO2使测定结果准确;
④若沉淀样品的质量为m g,若沉淀样品为纯净物,则判断沉淀为CuCO3,装置D的质量增加了n g,为二氧化碳气体质量,依据碳元素守恒得到mg=
| n |
| 44 |
mg-
| ||
| mg |
m-
| ||
| m |
故答案为:31n=11m;
m-
| ||
| m |
点评:本题考查了实验探究物质组成的实验设计和方案分析判断,装置特征分析,物质性质的分析应用是解题关键,实验基本操作和流程理解是解题关键,题目难度中等.

练习册系列答案
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
稀土是工业味精,邓小平说过“中东有石油,我们有稀土”.稀土元素铈(Ce)主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应.已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+.下列说法正确的是( )
| A、已知Ce原子序数是58,则其为镧系元素 | ||||||||
B、铈有四种稳定的核
| ||||||||
| C、用Ce(SO4)2溶液可与硫酸亚铁溶液反应,其离子方程式为:Ce4++2Fe2+=Ce3++2Fe3+ | ||||||||
| D、铈溶于氢碘酸的化学方程式可表示为:Ce+4HI=CeI4+2H2↑ |
下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
| A、Na2CO3溶液中:c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) |
| B、25℃,pH=7的NH3?H2O和NH4Cl的混合溶液中:c(Cl-)=c(NH4+)>c(H+)=c(OH-) |
| C、CH3COONa溶液中:c(Na+)>c(CH3COO -)>c(H+)>c(OH-) |
| D、NaHCO3溶液中:c(Na+)+c(H+)=c(OH-)+c(CO32-)+c(HCO3-) |
下列关于丙烯(CH3-CH=CH2)的说法正确的是( )
| A、丙烯分子有7个δ键,1个π键 |
| B、丙烯分子中3个碳原子都是sp3杂化 |
| C、丙烯分子中所有原子在同一平面上 |
| D、丙烯能使酸性高锰酸钾褪色 |
 水杨酸酯E为紫外线吸收剂,可用于配制防晒霜.E的一种合成路线如下:
水杨酸酯E为紫外线吸收剂,可用于配制防晒霜.E的一种合成路线如下: