��Ŀ����
2��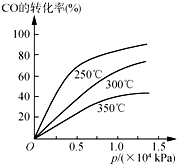 ��ҵ��һ�����ܱ������в������з�Ӧ�ϳɼ״���
��ҵ��һ�����ܱ������в������з�Ӧ�ϳɼ״���CO��g��+2H2��g��?CH3OH��g����
��1����ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ��ʾ��
�ٸ÷�Ӧ��H��0 ���������������ͬ������S��0����÷�Ӧ��һ�����һ������һ��������һ���������Է�����
��ʵ����������������250�桢l.3��l04kPa���ң�����Ϊѡ���ѹǿ�������Ǹ�ѹǿ�£�COת�����ѽϸߣ�90%���ң���������ѹǿCOת������߲����������ɱ����ӣ�
��2��ij�¶��£���2mol CO��6mol H2����2L���ܱ������У�3���Ӻﵽƽ��״̬�����c��CO��=0.1mol•L -1��
�ٷ�Ӧ��ʼ3min��H2��ƽ����Ӧ����Ϊ0.6mol/��L•min�����÷�Ӧ��ƽ�ⳣ��K=6.25��
���������������������£����������ѹ����ԭ����$\frac{1}{2}$���ﵽ��ƽ��ʱ����ԭƽ����ȣ������й�˵����ȷ����bc������ĸ����
a��������Ũ�ȼ��� b������Ӧ���ʼӿ죬�淴Ӧ����Ҳ�ӿ�
c���״������ʵ������� d��n��H2��/n��CH3OH������
���� ��1������ͼ���֪��ѹǿһ��ʱ���¶�Խ��CO��ת����ԽС��˵�������¶�ƽ�����淴Ӧ�����ƶ����ݴ��жϡ�H�����ݷ�Ӧǰ���������ʵ����ı仯�жϡ�S�����ݡ�G=��H-T��S�жϷ�Ӧ�Է������⣻
����ͼ��֪����250�桢1.3��104kPa���ң�COת�����ѽϸߣ���90%���ң�������ѹǿCOת������߲����������ɱ����ӣ�
��2���ٸ���v=$\frac{��c}{��t}$���м���3min��H2��ƽ����Ӧ���ʣ���������ʽ����ƽ��ʱ����ֵ�ƽ��Ũ�ȣ��ٸ���k=$\frac{c��C{H}_{3}OH��}{c��CO����{c}^{2}��{H}_{2}��}$���㣻
������ѹǿ�������淴Ӧ���ʶ�����ƽ��������Ӧ����ƽ��ʱ����ֵ�Ũ�ȶ����ݴ��жϣ�
��� �⣺��1������ͼ���֪��ѹǿһ��ʱ���¶�Խ��CO��ת����ԽС��˵�������¶�ƽ�����淴Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ������H��0��
�÷�Ӧ����Ӧ���������ʵ�����С�ķ�Ӧ�����ؼ�С������S��0��
�ɡ�G=��H-T��S��0����Ӧ�Է����У���֪�÷�Ӧ�ڵ��������Է����У������²����Է����У��÷�Ӧ��һ���Է����У�
�ʴ�Ϊ������������һ����
����ͼ��֪����250�桢1.3��104kPa���ң�COת�����ѽϸߣ���90%���ң�������ѹǿCOת������߲����������ɱ����ӣ���ʵ����������������1.3��104kPa���ң�
�ʴ�Ϊ����ѹǿ�£�COת�����ѽϸߣ�90%���ң���������ѹǿCOת������߲����������ɱ����ӣ�
��2����2molCO��6molH2����2L���ܱ������У�CO��H2����ʼŨ�ȷֱ�Ϊ$\frac{2mol}{2L}$=1mol/L��$\frac{6mol}{2L}$=3mol/L����ַ�Ӧ�ﵽƽ��ʱ���c��CO��=0.1 mol/L��COŨ�ȱ仯Ϊ1mol/L-0.1mol/L=0.9mol/L����
CO��g��+2H2��g��?CH30H��g��
��ʼ��mol/L����1 3 0
�仯��mol/L����0.9 1.8 0.9
ƽ�⣨mol/L����0.1 1.2 0.9
3min��H2��ƽ����Ӧ����v��H2��=$\frac{��c}{��t}$=$\frac{1.8mol/L}{3min}$=0.6mol/��L•min�����ʸ��¶��£��÷�Ӧ��ƽ�ⳣ��k=$\frac{0.9}{0.1��1��{2}^{2}}$=6.25��
�ʴ�Ϊ��0.6mol/��L•min����6.25��
��a������ѹǿ��ƽ��ʱ������Ũ������a����
b������ѹǿ����Ӧ��������Ũ�ȶ����������淴Ӧ���ʶ��ӿ죬��b��ȷ��
c������ѹǿƽ��������Ӧ�����ƶ����״������ʵ������ӣ���c��ȷ��
d������ѹǿƽ��������Ӧ�����ƶ������������ʵ�����С���״������ʵ�����������ƽ��ʱK=$\frac{c��C{H}_{3}OH��}{c��CO����{c}^{2}��{H}_{2}��}$��С����d����
�ʴ�Ϊ��bc��
���� �����ۺϿ��黯ѧƽ�����⣬�漰��ѧ��Ӧ�Է����жϡ���ѧƽ�ⳣ������ѧƽ��Ӱ�����صȣ����ջ�ѧƽ��ԭ��������Ӧ���ǽ��ؼ�����Ŀ�Ѷ��еȣ�

| A�� | CsICl2�����ڻ�ѧ�ϵķ���ɸ���������������������л�ԭ�ԣ�CsICl2�л�ԭ������Ϊ�н�ǿ��ԭ�Ե�I- | |
| B�� | ������ʮһ�š�����ɴ��ɹ��롰�칬���š��Խӣ���̫���ܹ��ز����ǹ� | |
| C�� | ˾ĸ�춦���������װ塢������̼�ܸ��۾���ܵ�ԭ�������Ͻ� | |
| D�� | ���������º��͵��������͵����ǽ������� |
 |  |  |  |
| A�����հ��� | B���к��ȵIJⶨ | C�������屽�ͱ��Ļ���� | D����ȥSO2�����е�HCl |
| A�� | A | B�� | B | C�� | C | D�� | D |
| X�� | Y�� | |
| Z�� |
| A�� | Y�ĵ�����ˮ��Ӧʱ��Y�ĵ��ʼ������������ǻ�ԭ�� | |
| B�� | X������������Ӧ��ˮ����������̬�⻯����Է�Ӧ������ | |
| C�� | X��Y��ZԪ���γɵĵ��ʣ�������Z���ʵķе���� | |
| D�� | X���⻯��ֻ��һ�� |
�������ˮ�м������BaCl2��Һ�����ˣ�
����������Һ�м������Na2CO3��Һ�����ˣ�
����Һ���������pH�����һ�ξ�����ˮ��
��1�����̢��ȥ��������SO42-����Ӧ�����ӷ���ʽ��Ba2++SO42-�TBaSO4����
��2�����̢����ɵIJ��ֳ��������ܽ�ȣ�20��/g�������
| CaSO4 | Mg2��OH��2CO3 | CaCO3 | BaSO4 | BaCO3 |
| 2.6��10-2 | 2.5��10-4 | 7.8��10-4 | 2.4��10-4 | 1.7��10-3 |
�ڳ�ȥMg2+�����ӷ���ʽ��2Mg2++2CO32-+H2O�TMg2��OH��2CO3��+CO2��
��3���ڶ��ξ���Ҫ��ȥ����I-��IO3-��NH4+��Ca2+��Mg2+������ʾ����ͼ��
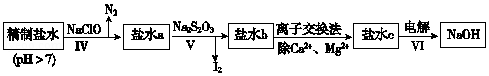
���̢���ȥ��������NH4+��I-��
| A�� | ͬ���칹����ֻ�������л��������֮�� | |
| B�� | ͬ���칹������������֮�� | |
| C�� | ������������л��������һ������ͬ���칹���� | |
| D�� | ������������л����������ܴ���ͬ���칹���� |
| A�� | 8�� | B�� | 10�� | C�� | 11�� | D�� | 12�� |