题目内容
3.某太阳能电池的工作原理如图所示.下列说法不正确的是( )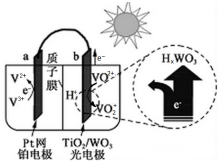
| A. | 光照时,太阳能主要转化为电能 | |
| B. | 光照时,b极的电极反应式为VO2+-e-+H2O═VO2++2H+ | |
| C. | 光照时,每转移5 mol电子,有5mol H+由b极区向a极区迁移 | |
| D. | 夜间,a极的电极反应式为V3++e-═V2+ |
分析 A.太阳能电池是将太阳能转化为电能;
B.光照时,b极上VO2+失电子发生氧化反应;
C.根据电荷守恒判断;
D.夜间无光照时,相当于蓄电池放电,a极上V2+失电子.
解答 解:A.太阳能电池是将太阳能转化为电能,从而实现太阳能的利用,故A正确;
B.光照时,b极上VO2+失电子发生氧化反应,b极反应为VO2++H2O-e-=VO2++2H+,故B正确;
C.根据电荷守恒可知,每转移5 mol电子,即有5mol负电荷转移,则有5mol正电荷转移,所以有5mol H+由b极区向a极区迁移,故C正确;
D.夜间无光照时,相当于蓄电池放电,a极的电极反应式为:V2+-e-=V3+,故D错误.
故选D.
点评 本题考查原电池知识,侧重于原电池的工作原理的考查,注意把握电极反应的判断,把握电极方程式的书写,为解答该类题目的关键,难度不大.

练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目
14.下列过程放出热量的是( )
| A. | 液氨气化 | B. | 钠与水反应 | C. | 碳酸钙分解 | D. | 化学键的断裂 |
11.下列关于有机化合物的叙述说法不正确的是( )
| A. | 等质量的A、B两种烃分别完全燃烧后,生成的CO2与消耗的O2的物质的量均相同,则A和B一定互为同系物 | |
| B. | 沸点比较:正戊烷>异戊烷>新戊烷 | |
| C. | 乙酸与乙醇在一定条件下反应生成乙酸乙酯和水的反应属于取代反应 | |
| D. | 判断苯分子中不存在碳碳单键与碳碳双键的交替结构的依据是:邻二甲苯只有一种结构 |
8. 工业燃烧煤、石油等化石燃料释放出大量NOx、CO、CO2等气体,严重污染空气,对废气进行脱硝,脱碳等处理可实现绿色环保、废物利用.
工业燃烧煤、石油等化石燃料释放出大量NOx、CO、CO2等气体,严重污染空气,对废气进行脱硝,脱碳等处理可实现绿色环保、废物利用.
Ⅰ、脱硝:
已知:①H2的热值为142.9kJ/g(热值是表示单位质量的燃料完全燃烧生成稳定的化合物时所放出的热量);
②N2(g)+2O2(g)═2NO2(g)△H=+133kJ/mol
③H2O(g)═H2O(1)△H=-44kJ/mol
则催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为4H2(g )+2NO2( g)=N2(g )+4H2O(g)△H=-1100.2KJ/mol;
Ⅱ、脱碳
(1)CO与空气可设计成燃料电池(以熔融的碳酸盐为电解质).写出该电池的负极反应式:CO-2e-+CO32-=2CO2.
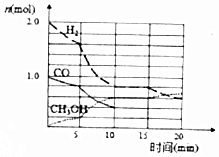
(2)甲醇是一种可再生能源,工业上可用合成气制备甲醇,反应为CO(g)+2H2(g)?CH3OH(g).某温度下在容积为VL的密闭容器中进行反应,其相关数据如图;反应开始至平衡时,用H2表示化学反应速率为$\frac{0.12}{V}$mol ( L•min ).该温度下CO的平衡转化率为60%.
(3)向1L密闭容器中加入1molCO2、3molH2,在适当的条件下,发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g).
①下列叙述能说明此反应达到平衡状态的是abe.
a.混合气体的平均相对分子质量保持不变
b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等
d.混合气体的密度保持不变
e.1molCO2生成的同时又3molH-H键断裂
②相同条件下,在容积都为1L且固定的两个密闭容器中,按如下方式加入反应物,一段时间后反应达到平衡.
若甲中平衡后气体的压强为开始的0.6倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆向反应方向进行,则b的取值可能为b (填序号)
a.0.7 b.0.9 c.1.2
若保持温度不变,起始加入0.5molCO2、0.5molH2、0.5molCH3OH(g)、0.5molH2O(g) 则此反应速率的关系:v正> v逆.(填“>”、“<”或“=”)
 工业燃烧煤、石油等化石燃料释放出大量NOx、CO、CO2等气体,严重污染空气,对废气进行脱硝,脱碳等处理可实现绿色环保、废物利用.
工业燃烧煤、石油等化石燃料释放出大量NOx、CO、CO2等气体,严重污染空气,对废气进行脱硝,脱碳等处理可实现绿色环保、废物利用.Ⅰ、脱硝:
已知:①H2的热值为142.9kJ/g(热值是表示单位质量的燃料完全燃烧生成稳定的化合物时所放出的热量);
②N2(g)+2O2(g)═2NO2(g)△H=+133kJ/mol
③H2O(g)═H2O(1)△H=-44kJ/mol
则催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为4H2(g )+2NO2( g)=N2(g )+4H2O(g)△H=-1100.2KJ/mol;
Ⅱ、脱碳
(1)CO与空气可设计成燃料电池(以熔融的碳酸盐为电解质).写出该电池的负极反应式:CO-2e-+CO32-=2CO2.
(2)甲醇是一种可再生能源,工业上可用合成气制备甲醇,反应为CO(g)+2H2(g)?CH3OH(g).某温度下在容积为VL的密闭容器中进行反应,其相关数据如图;反应开始至平衡时,用H2表示化学反应速率为$\frac{0.12}{V}$mol ( L•min ).该温度下CO的平衡转化率为60%.
(3)向1L密闭容器中加入1molCO2、3molH2,在适当的条件下,发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g).
①下列叙述能说明此反应达到平衡状态的是abe.
a.混合气体的平均相对分子质量保持不变
b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等
d.混合气体的密度保持不变
e.1molCO2生成的同时又3molH-H键断裂
②相同条件下,在容积都为1L且固定的两个密闭容器中,按如下方式加入反应物,一段时间后反应达到平衡.
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1mol CO2、3molH2 | amol CO2、3amolH2 bmolCH3OH(g)、bmolH2O(g) |
a.0.7 b.0.9 c.1.2
若保持温度不变,起始加入0.5molCO2、0.5molH2、0.5molCH3OH(g)、0.5molH2O(g) 则此反应速率的关系:v正> v逆.(填“>”、“<”或“=”)
15.下列化学方程式不正确的是( )
| A. | CH3CO18OC2H5+H2O $?_{△}^{稀硫酸}$ CH3COOH和C2H518OH | |
| B. | 溴乙烷与氢氧化溶液共热:CH3CH2Br+NaOH $→_{△}^{水}$ CH3CH2OH+NaBr | |
| C. | 蔗糖水解: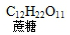 +H2O$\stackrel{催化剂}{→}$ +H2O$\stackrel{催化剂}{→}$ | |
| D. | 苯酚钠中通入二氧化碳: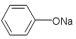 +CO2+H2O→ +CO2+H2O→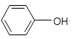 +NaHCO3 +NaHCO3 |
3.某电池以K2FeO4和Zn为电极材料,KOH溶液为电解溶质溶液.下列说法正确的是( )
| A. | Zn为电池的正极 | |
| B. | 负极反应式为2FeO42-+10H++6e-═Fe2O3+5H2O | |
| C. | 该电池使用完不可随便丢弃,应深埋地下 | |
| D. | 电池工作时OH-向负极迁移 |
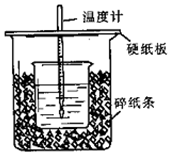 50 mL 0.50 mol•L-1盐酸与50 mL 0.55 mol•L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50 mL 0.50 mol•L-1盐酸与50 mL 0.55 mol•L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: )的一条路线如图:
)的一条路线如图: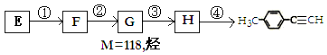
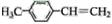 .
. 、
、 .
. 西兰花营养丰富,含蛋白质、淀粉、油脂、叶酸、维生素C和叶绿素,营养成份位居同类蔬菜之首,被誉为“蔬菜皇冠”.
西兰花营养丰富,含蛋白质、淀粉、油脂、叶酸、维生素C和叶绿素,营养成份位居同类蔬菜之首,被誉为“蔬菜皇冠”.