题目内容
3.某电池以K2FeO4和Zn为电极材料,KOH溶液为电解溶质溶液.下列说法正确的是( )| A. | Zn为电池的正极 | |
| B. | 负极反应式为2FeO42-+10H++6e-═Fe2O3+5H2O | |
| C. | 该电池使用完不可随便丢弃,应深埋地下 | |
| D. | 电池工作时OH-向负极迁移 |
分析 某电池以K2FeO4和Zn为电极材料,KOH溶液为电解溶质溶液,原电池发生工作时,Zn被氧化,为原电池的负极,K2FeO4具有氧化性,为正极,碱性条件下被还原生成Fe(OH)3,结合电极方程式以及离子的定向移动解答该题.
解答 解:A.原电池发生工作时,Zn被氧化,为原电池的负极,故A错误;
B.KOH溶液为电解质溶液,则正极电极方程式为2FeO42-+6e-+8H2O=2Fe(OH)3+10OH-,故B错误;
C.该电池含有重金属元素,埋在地下会污染地下水,故C错误;
D.电池工作时阴离子OH-向负极迁移,故D正确.
故选D.
点评 本题考查原电池知识,侧重考查学生的分析能力,题目较为基础,注意从元素化合价的角度分析,把握原电池与氧化还原反应的关系,难度不大.

练习册系列答案
 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
3.某太阳能电池的工作原理如图所示.下列说法不正确的是( )
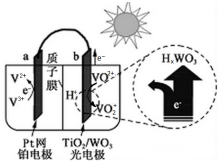

| A. | 光照时,太阳能主要转化为电能 | |
| B. | 光照时,b极的电极反应式为VO2+-e-+H2O═VO2++2H+ | |
| C. | 光照时,每转移5 mol电子,有5mol H+由b极区向a极区迁移 | |
| D. | 夜间,a极的电极反应式为V3++e-═V2+ |
4.化学是你,化学是我,化学深入我们生活,下列说法正确的是( )
| A. | 苯甲酸和苯甲酸钠都是食品防腐剂 | |
| B. | 食用花生油和汽油都属于酯 | |
| C. | 包装用材料聚乙烯和聚氯乙烯都属于烃 | |
| D. | 毛发、鸡蛋清都不能发生水解反应 |
8. 维生素是人体需要的营养物质.图为某品牌维生素C泡腾片说明书的部分内容.该泡腾片中添加的着色剂是喹啉黄,甜味剂是糖精钠.泡腾片溶于水时产生“沸腾”效果,是由于添加的酒石酸和碳酸氢钠反应释放出了气体.
维生素是人体需要的营养物质.图为某品牌维生素C泡腾片说明书的部分内容.该泡腾片中添加的着色剂是喹啉黄,甜味剂是糖精钠.泡腾片溶于水时产生“沸腾”效果,是由于添加的酒石酸和碳酸氢钠反应释放出了气体.
 维生素是人体需要的营养物质.图为某品牌维生素C泡腾片说明书的部分内容.该泡腾片中添加的着色剂是喹啉黄,甜味剂是糖精钠.泡腾片溶于水时产生“沸腾”效果,是由于添加的酒石酸和碳酸氢钠反应释放出了气体.
维生素是人体需要的营养物质.图为某品牌维生素C泡腾片说明书的部分内容.该泡腾片中添加的着色剂是喹啉黄,甜味剂是糖精钠.泡腾片溶于水时产生“沸腾”效果,是由于添加的酒石酸和碳酸氢钠反应释放出了气体.
12.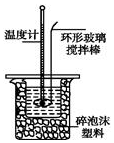 某实验小组用0.50mol•L-1NaOH溶液和0.50mol•L-1硫酸溶液进行中和热的测定.
某实验小组用0.50mol•L-1NaOH溶液和0.50mol•L-1硫酸溶液进行中和热的测定.
Ⅰ.配制0.50mol•L-1NaOH溶液
(1)若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体5.0g.
(2)从图中选择称量NaOH固体所需要的仪器是(填字母):abe.
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示.
(1)不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是Cu传热快,热量损失大.
(2)在操作正确的前提下,提高中和热测定准确性的关键是减少实验过程中的热量损失.大烧杯如不盖硬纸板,求得的中和热数值将偏小(填“偏大”、“偏小”或“无影响”).结合日常生活实际该实验在保温杯中(家用产品)效果更好.
(3)写出该反应中和热的热化学方程式:(中和热为57.3kJ•mol-1)$\frac{1}{2}$H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol;.
(4)取50mLNaOH溶液和30mL硫酸溶液进行实验,实验数据如表.
①表中的温度差平均值为4.0℃.
②近似认为0.50mol•L-1 NaOH溶液和0.50mol•L-1硫酸溶液的密度都是1g•cm-3,中和后生成溶液的比热容c=4.18J•(g•℃)-1.则中和热△H=-53.5kJ/mol(取小数点后一位).
③上述实验数值结果与57.3kJ•mol-1有偏差,产生偏差的原因可能是(填字母)acd.
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
④实验中改用60mL0.5mol/L盐酸跟50mL0.55mol•L-1氢氧化钠进行反应,与上述实验相比,所放出的热量不相等(填相等或不相等,下同),所求的中和热相等简述理由中和热是指酸跟碱发生中和反应生成1mol水所放出的热量为标准的,而与酸、碱的用量无关..
 某实验小组用0.50mol•L-1NaOH溶液和0.50mol•L-1硫酸溶液进行中和热的测定.
某实验小组用0.50mol•L-1NaOH溶液和0.50mol•L-1硫酸溶液进行中和热的测定.Ⅰ.配制0.50mol•L-1NaOH溶液
(1)若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体5.0g.
(2)从图中选择称量NaOH固体所需要的仪器是(填字母):abe.
| 名称 | 托盘天平 (带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |
(1)不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是Cu传热快,热量损失大.
(2)在操作正确的前提下,提高中和热测定准确性的关键是减少实验过程中的热量损失.大烧杯如不盖硬纸板,求得的中和热数值将偏小(填“偏大”、“偏小”或“无影响”).结合日常生活实际该实验在保温杯中(家用产品)效果更好.
(3)写出该反应中和热的热化学方程式:(中和热为57.3kJ•mol-1)$\frac{1}{2}$H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol;.
(4)取50mLNaOH溶液和30mL硫酸溶液进行实验,实验数据如表.
| 试验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.6 | |
| 2 | 27.0 | 27.4 | 27.2 | 31.2 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50mol•L-1 NaOH溶液和0.50mol•L-1硫酸溶液的密度都是1g•cm-3,中和后生成溶液的比热容c=4.18J•(g•℃)-1.则中和热△H=-53.5kJ/mol(取小数点后一位).
③上述实验数值结果与57.3kJ•mol-1有偏差,产生偏差的原因可能是(填字母)acd.
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
④实验中改用60mL0.5mol/L盐酸跟50mL0.55mol•L-1氢氧化钠进行反应,与上述实验相比,所放出的热量不相等(填相等或不相等,下同),所求的中和热相等简述理由中和热是指酸跟碱发生中和反应生成1mol水所放出的热量为标准的,而与酸、碱的用量无关..




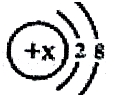 当x=8时,该粒子符号为O2-;当x=11时,该粒子符号为Na+;当x=13时,写出该粒子的硝酸盐的化学式为Al(NO3)3.
当x=8时,该粒子符号为O2-;当x=11时,该粒子符号为Na+;当x=13时,写出该粒子的硝酸盐的化学式为Al(NO3)3.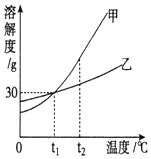 图是甲、乙两种固体物质的溶解度曲线.
图是甲、乙两种固体物质的溶解度曲线.