题目内容
11.下列关于有机化合物的叙述说法不正确的是( )| A. | 等质量的A、B两种烃分别完全燃烧后,生成的CO2与消耗的O2的物质的量均相同,则A和B一定互为同系物 | |
| B. | 沸点比较:正戊烷>异戊烷>新戊烷 | |
| C. | 乙酸与乙醇在一定条件下反应生成乙酸乙酯和水的反应属于取代反应 | |
| D. | 判断苯分子中不存在碳碳单键与碳碳双键的交替结构的依据是:邻二甲苯只有一种结构 |
分析 A.等质量的A、B两种烃分别完全燃烧后,生成的CO2与消耗的O2的物质的量均相同,C、H的质量分数相同;
B.相同碳原子数时,支链越多,沸点越低;
B.酯化反应为取代反应;
D.邻二甲苯只有一种结构,可知苯中不存在但、双键.
解答 解:A.等质量的A、B两种烃分别完全燃烧后,生成的CO2与消耗的O2的物质的量均相同,C、H的质量分数相同,如为苯、乙炔,二者不是同系物,故A错误;
B.相同碳原子数时,支链越多,沸点越低,则沸点比较:正戊烷>异戊烷>新戊烷,故B正确;
B.酯化反应为取代反应,则乙酸与乙醇在一定条件下反应生成乙酸乙酯和水的反应属于取代反应,故C正确;
D.邻二甲苯只有一种结构,可知苯中不存在但、双键,则判断苯分子中不存在碳碳单键与碳碳双键的交替结构,故D正确;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意选项A为易错点,题目难度不大.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
1.将1.52g铜镁合金完全溶解于50mL密度为1.40g•mL-1、质量分数为63%的浓硝酸得到NO2和N2O4的混合气体1120mL(标准状况),向反应后的溶液中加入1.0mol•L-1NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的是( )
| A. | 该合金中铜与镁的物质的量之比是2:1 | |
| B. | 该浓硝酸中HNO3的物质的量浓度是14.0 mol•L-1 | |
| C. | 得到2.54g沉淀时,加入NaOH溶液的体积是600L | |
| D. | NO2和N2O4的混合气体中,NO2的体积分数是80% |
19.下列关于有机物的说法正确的是( )
| A. | 苯分子中无碳碳双键,苯不能发生加成反应 | |
| B. | 甲烷能与氯水发生取代反应 | |
| C. | 乙醇在一定条件下能被氧化成乙醛 | |
| D. | 乙烯和苯均能与溴水反应而使其褪色 |
16.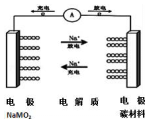 C-NaMO2电池是科学家正在研发的钠离子电池,据悉该电池可以将传统锂电池的续航能力提升7倍.该电池的电池反应式为:NaMO2+nC?Na(1-x)MO2+NaxCn,下列有关该电池的说法正确的是( )
C-NaMO2电池是科学家正在研发的钠离子电池,据悉该电池可以将传统锂电池的续航能力提升7倍.该电池的电池反应式为:NaMO2+nC?Na(1-x)MO2+NaxCn,下列有关该电池的说法正确的是( )
 C-NaMO2电池是科学家正在研发的钠离子电池,据悉该电池可以将传统锂电池的续航能力提升7倍.该电池的电池反应式为:NaMO2+nC?Na(1-x)MO2+NaxCn,下列有关该电池的说法正确的是( )
C-NaMO2电池是科学家正在研发的钠离子电池,据悉该电池可以将传统锂电池的续航能力提升7倍.该电池的电池反应式为:NaMO2+nC?Na(1-x)MO2+NaxCn,下列有关该电池的说法正确的是( )| A. | 电池放电时,溶液中钠离子向负极移动 | |
| B. | 电池充电时的阳极反应式为:nC+x Na+-xe-═NaxCn | |
| C. | 消耗相同质量金属时,用锂作负极产生电子的物质的量比用钠时少 | |
| D. | 该电池负极的电极反应为:NaMO2-xe-═Na(1-x)MO2+xNa+ |
3.某太阳能电池的工作原理如图所示.下列说法不正确的是( )
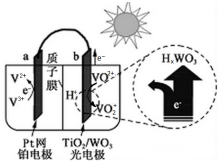

| A. | 光照时,太阳能主要转化为电能 | |
| B. | 光照时,b极的电极反应式为VO2+-e-+H2O═VO2++2H+ | |
| C. | 光照时,每转移5 mol电子,有5mol H+由b极区向a极区迁移 | |
| D. | 夜间,a极的电极反应式为V3++e-═V2+ |

 +HCl
+HCl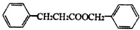 ;检验M中官能团的试剂是银氨溶液或新制备氢氧化铜浊液.
;检验M中官能团的试剂是银氨溶液或新制备氢氧化铜浊液.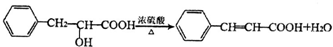 ,
, .
.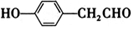 .
.