题目内容
5.药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得: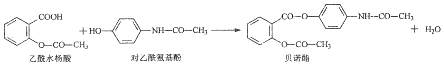
下列有关叙述不正确的是( )
| A. | 贝诺酯分子中有2种含氧官能团 | |
| B. | 可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚 | |
| C. | lmol乙酰水杨酸最多消耗3molNaOH | |
| D. | 贝诺酯与足量NaOH溶液共热,最终生成乙酰水杨酸钠和对乙酰氮基酚钠 |
分析 A.贝诺酯分子中含-COOC-、-CONH-两种官能团;
B.对乙酰氨基酚含酚-OH,可与氯化铁发生显色反应;
C.乙酰水杨酸的羧基、酯基都可与氢氧化钠溶液反应;
D.贝诺酯与足量NaOH溶液共热,-COOC-、-CONH-均发生水解
解答 解:A.贝诺酯分子中含-COOC-、-CONH-两种官能团,故A正确;
B.对乙酰氨基酚含酚-OH,可与氯化铁发生显色反应,则可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚,故B正确;
C.乙酰水杨酸的羧基、酯基都可与氢氧化钠溶液反应,且酯基可水解生成酚羟基和羧基,则lmol乙酰水杨酸最多消耗3molNaOH,故C正确;
D.贝诺酯与足量NaOH溶液共热,-COOC-、-CONH-均发生水解,不会生成乙酰水杨酸钠和对乙酰氨基酚,故D错误;
故选D.
点评 本题考查有机物的结构和性质,为高频考点,明确酚及酯的性质是解答本题的关键,注意选项D中的水解为解答的难点和易错点,题目难度中等.

练习册系列答案
相关题目
16.下列有关有机物的说法正确的是( )
| A. | 蛋白质溶液中加Na2SO4可使其变性 | |
| B. | 乙烷、苯、葡萄糖溶液均不能使酸性KMnO4溶液褪色 | |
| C. | 有机物CH2=CHCH(CH3)Cl能发生加成反应、取代反应、缩聚反应、氧化反应 | |
| D. | 分子式为C4H7ClO2且能与NaHCO3反应放出气体的有机物结构有5种(不包含立体异构) |
13.化学与科技、社会、生活有着密切的联系.下列有关说法正确的是( )
| A. | 用于消除H7N9病毒的漂白粉是一种强电解质 | |
| B. | 古代制盐(NaCl)有“东晒西煮”之说,是利用了复杂的物理、化学方法 | |
| C. | 铜带(镀锡)是光伏电池的电子元件,破损时不加快其腐蚀 | |
| D. | 纤维素、蛋白质和油脂均可发生水解,都属于天然高分子化合物 |
20.下列关于有机化合物的说法正确的是( )
| A. | 乙醇室温下在水中的溶解度小于溴苯 | |
| B. | 氨基酸和蛋白质遇硫酸铜溶液均会变性 | |
| C. | 石油裂化和油脂皂化均是由高分子物质生成小分子物质的过程 | |
| D. | 苯和氯乙烯均能发生加成反应 |
10.设NA为阿伏加德罗常数值,下列说法正确的是( )
| A. | 标准状况下,2.24 L CC14所含的原子数为0.5 NA | |
| B. | 0.1 mol FeCl3水解生成的Fe(OH)3胶粒数为0.1 NA | |
| C. | 将lmol Cl2通人水中,HC1O、Cl-、C1O-粒子数之和为2 NA | |
| D. | 11.2 g 铁粉与足量稀硝酸反应失去电子数一定为0.6 NA |
17.在透明的酸性溶液中能大量共存的离子组是( )
| A. | Ba2+、K+、OH-、NO3- | B. | NH4+、Cu2+、SO42-、Cl- | ||
| C. | Al3+、Fe2+、SO42-、NO3- | D. | Na+、Ca2+、Cl-、CO32- |
9.下列有关说法不正确的是( )
| A. | “凡造竹纸…用上好石灰化汁涂浆”,造纸利用了石灰的碱性 | |
| B. | “曾青(硫酸铜)涂铁,铁赤色如铜”,过程中发生了罝换反应 | |
| C. | 人民币防伪荧光油墨由颜料与树脂连接料等制成,其中树脂属于有机高分子材料 | |
| D. | 含钙镁离子的硬水均可通过煮沸的方法使之软化 |
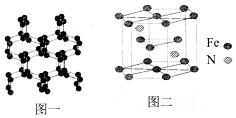 南京理工大学化工学院胡炳成教授团队于2017年1月成功合成世界首个全氮阴离子盐,使氮原子簇化合物的研究又有了新的突破.请根据材料回答以下问题:
南京理工大学化工学院胡炳成教授团队于2017年1月成功合成世界首个全氮阴离子盐,使氮原子簇化合物的研究又有了新的突破.请根据材料回答以下问题: .
.