题目内容
17.某矿石中除含SiO2外,还有9.24%CoO、2.78%Fe2O3、0.96%MgO、0.084%CaO,从该矿石中提取钴的主要流程如图1: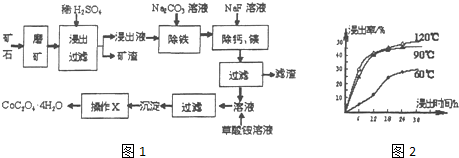
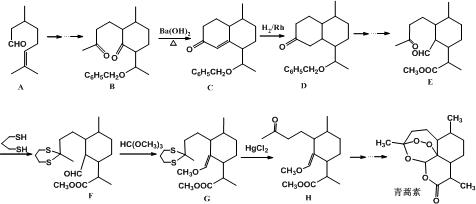
(1)在一定浓度的H2SO4溶液中,钴的浸出率随时间、温度的变化如图2所示.考虑生产成本和效率,最佳的浸泡时间为12h,最佳的浸出温度为90℃.
(2)请配平下列除铁的化学方程式:
□Fe(SO4)3+□H2O+□Na2CO3═□Na2SO4+□CO2↑+□Na2Fe6(SO4)4(OH)12↓
(3)“除钙、镁”的反应原理如下:
MgSO4+2NaF═MgF2↓+Na2SO4 CaSO4+2NaF═CaF2↓+Na2SO4
已知Ksp(CaF2)=1.11×10-10、Ksp(MgF2)=7.40×10-11,加入过量NaF溶液反应完全后过滤,则滤液中的c(Ca2+)c(Mg2+)=1.5.
(4)“沉淀”表面吸附的主要离子有SO42-、NH4+、Na+、F-;“操作X”名称为洗涤、干燥.
(5)某锂离子电池正极是LiCoO2,以含Li+的导电固体为电解质.充电时,Li+还原为Li,并以原子形式嵌入电池负极材料C6中,电池反应为:LiCoO2+C6?放电充电CoO2+LiC6则LiC6中Li的化合价为0价.若放电时有1mol e-转移,正极质量增加7g.
分析 水钴矿磨矿将矿石粉碎,增大接触面积,加快反应速率,加入稀硫酸,矿渣为SiO2,滤液中含有:CoSO4、Fe2(SO4)3、MgSO4、CaSO4,加入碳酸钠,除去Fe2(SO4)3,加入氟化钠,除去钙镁,过滤得主要含CoSO4的溶液,加入草酸铵,通过沉淀、过滤、洗涤、干燥得到四水合草酸钴,
(1)根据浸出率与时间和温度的关系及生产成本分析,时间越长浸出率越高,温度越高,浸出率越高;
(2)根据原子守恒配平方程式,;
(3)依据溶度积常数计算,$\frac{c(C{a}^{2+})}{c(M{g}^{2+})}$×$\frac{c({F}^{-})}{c({F}^{-})}$=$\frac{Ksp(Ca{F}_{2})}{Ksp(Mg{F}_{2})}$;
(4)根据流程图中加入的物质分析,该沉淀中吸附易溶于水的离子;得到的沉淀要进行洗涤和干燥,才能得到较纯净、干燥的物质;
(5)放电时,该电池是原电池,正极上得电子发生还原反应,依据负极电极材料和题干信息分析计算.
解答 解:(1)根据图知,时间越长浸出率越高,温度越高,浸出率越高,但浸出12小时后,浸出率变化不大,90℃和120℃浸出率变化不大,且时间过长、温度过高导致成本较大,所以最佳的浸出时间为12小时,最佳的浸出温度为90℃,
故答案为:12;90;
(2)根据原子守恒配平方程式,所以其方程式为:3Fe2(SO4)3+6H2O+6Na2CO3=Na2Fe6 (SO4)4(OH)12↓+5Na2SO4+6CO2↑,
故答案为:3,6,6,1,5,6;
(3)已知Ksp(CaF2)=1.11×10-10、Ksp(MgF2)=7.40×10-11,加入过量NaF溶液反应完全后过滤,则滤液中$\frac{c(C{a}^{2+})}{c(M{g}^{2+})}$=$\frac{Ksp(Ca{F}_{2})}{Ksp(Mg{F}_{2})}$=$\frac{1.1×1{0}^{-10}}{7.40×1{0}^{-11}}$=1.5,
故答案为:1.5;
(4)该沉淀中吸附易溶于水的离子,根据流程图知,溶液中含有SO42-、NH4+、Na+、F-,所以沉淀上含有SO42-、NH4+、Na+、F-,得到的沉淀要进行洗涤和干燥才能得到较纯净、干燥的物质,
故答案为:SO42-、NH4+、Na+、F-;洗涤、干燥;
(5)放电时,该电池是原电池,正极上得电子发生还原反应,电极反应式为:CoO2+Li++e-=LiCoO2,充电时,Li+还原为Li,并以原子形式嵌入电池负极材料碳-6(C6)中,所以负极为LiC6中Li的化合价为0价,若放电时有1mol e-转移,CoO2+Li++e-=LiCoO2,正极质量增加为1molLi+的质量=1mol×7g/mol=7g;
故答案为:0;7.
点评 本题考查难溶电解质的溶解平衡、电极反应式的书写、物质的分离和提纯等知识点,难点是(3)题,明确溶度积常数的含义是解此题关键,电极反应式的书写是学习难点,要结合电解质溶液的酸碱性书写,难度中等.

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案| A. | 升高温度,v(正)变大,v(逆)变小 | |
| B. | 恒温恒容,平衡前后混合气体的密度保持不变 | |
| C. | 恒温恒压,充入N2,平衡不移动 | |
| D. | 恒温恒容,充入O2,O2的转化率升高 |
| A. | 用广泛pH试纸测得0.05mol•L-1 H2SO4溶液的pH=1 | |
| B. | 做焰色反应实验时,透过蓝色钴玻璃,观察到火焰颜色为紫色,证明被检验物一定为钾盐 | |
| C. | 滴定过程中,眼睛要始终注视锥形瓶中液体的颜色变化 | |
| D. | 配制FeSO4溶液时,先将FeSO4固体溶解在稀硫酸中,然后稀释到所需浓度,最后再加入少量铁粉 |
| A. | 标准状况下,11.2 L乙醇中含有的碳氢键数为2.5NA | |
| B. | 标准状况下电解硫酸铜溶液时,阳极每生成气体3.36 L,转移电子数为0.6NA | |
| C. | 标准状况下,30gNO和16gO2混合所生成的气体分子数为NA | |
| D. | 1mol氯气参加氧化还原反应,转移的电子数一定为2NA |
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | +3 | ||
| 其它 | 常温下该单质为黄色固体 | 无机非金属材料的主角 | 焰色反应呈黄色 | 其氧化物可做耐火材料 |
 .
.(2)X的氢化物的VSEPR模型为四面体.属于极性 (填“极性”或“非极性”)分子.
(3)根据表中数据推测,Y的原子半径的最小范围是大于0.099nm小于0.143nm.
(4)甲、乙是上述部分元素的最高价氧化物对应的水化物,且甲+乙→丙十水.若丙的水溶液呈碱性,则丙的化学式是NaAlO2.
(5)M的氢化物是常见溶剂,白色硫酸铜粉末溶解于其中能形成蓝色溶液,请解释原因:铜离子结合水分子变成水合铜离子.
(6)Z晶体的原子堆积模型为体心立方堆积,设Z原子半径为r cm,则Z晶体的密度为$\frac{2×23}{{N}_{A}(\frac{4r}{\sqrt{3}})^{3}}$g/cm3(写出表达式,假设阿伏加德罗常数为NA).
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
| A. | 粮食酿酒 | B. | 食物变质 | C. | 冰雪消融 | D. | 石油裂解 |
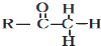 +
+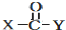 $\stackrel{OH-}{→}$
$\stackrel{OH-}{→}$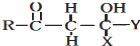
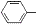 CH2CH2CHO)的路线流程图.路线流程图示例如下:
CH2CH2CHO)的路线流程图.路线流程图示例如下: .
.