��Ŀ����
20��ijͬѧ����ˮ�ʼ��վ����480mL 0.5mol•L-1 NaOH��Һ�Ա�ʹ�ã���1����ͬѧӦѡ��500mL������ƿ��
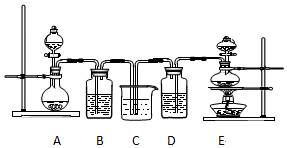
��2�������������ͼ��ʾ����ͼA����Ӧ�ڢ١���ͼ�е�C����ѡ����ĸ��֮�䣮

A�������B�������C�������
��3����ͬѧӦ��ȡNaOH����10.0 g��
��2���Тݵľ��������Һ���̶���1��2cmʱ���ý�ͷ�ιܵμ�����Һ����ʹ���̶�������
��4�����в�����������Һ��Ũ�ȴ�С�к�Ӱ�죿
��ת������Һ��δϴ�Ӳ��������ձ���Ũ�Ȼ�ƫС���ƫ��ƫС������Ӱ�족����ͬ����
������ƿ��ԭ������������ˮ��Ũ�Ȼ���Ӱ�죮
���� ��1������������Һ���ѡ����ʹ������ƿ��
��2������һ�����ʵ���Ũ����Һһ�㲽�裺���㡢�������ܽ⡢��Һ��ϴ�ӡ����ݡ�ҡ�ȣ��ݴ˽��
��3������m=CVM������Ҫ���ʵ����������ݶ��ݵ���ȷ�������
��4���������������ʵ����ʵ��������Һ�������Ӱ�죬����c=$\frac{n}{V}$�����жϣ�
��� �⣺��1������480mL 0.5mol•L-1 NaOH��Һ��Ӧѡ��500mL����ƿ��
�ʴ�Ϊ��500��
��2������һ�����ʵ���Ũ����Һһ�㲽�裺���㡢�������ܽ⡢��Һ��ϴ�ӡ����ݡ�ҡ�ȣ�ͼAΪϴ�Ӻ�������ˮ��Ӧ����ϴ�����ý�ͷ�ιܶ��ݲ���֮�䣬
��ѡ��C��
��3������480mL 0.5mol•L-1 NaOH��Һ��Ӧѡ��500mL����ƿ��ʵ������500mL��Һ����Ҫ���ʵ�����m=0.5L��0.5mol/L��40g/mol=10.0g��
���ݵ���ȷ����Ϊ��������ˮ��Һ���̶���1��2cmʱ���ý�ͷ�ιܵμ�����Һ����ʹ���̶������У�
�ʴ�Ϊ��10.0��Һ���̶���1��2cmʱ���ý�ͷ�ιܵμ�����Һ����ʹ���̶������У�
��4����ת������Һ��δϴ�Ӳ��������ձ����������ʲ�����ģ����ʵ����ʵ���ƫС����ҺŨ�Ȼ�ƫС��
�ʴ�Ϊ��ƫС��
������ƿ��ԭ������������ˮ�������ʵ����ʵ�������Һ������������Ӱ�죬��ҺŨ����Ӱ�죻
�ʴ�Ϊ����Ӱ�죮
���� ���⿼����һ�����ʵ���Ũ����Һ�����ƣ���ȷ����ԭ�������������ǽ���ؼ���ע������ƿ���ѡ��ע�ⶨ�ݵ���ȷ��������Ŀ�ѶȲ���

 ��ǰ����ϵ�д�
��ǰ����ϵ�д�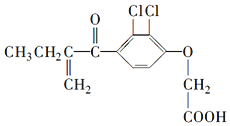
| A�� | ����������������������ķ���ʽ��C14H14Cl2O4 | |
| B�� | ����������ڴ���ͬһƽ���ԭ�Ӳ�����10�� | |
| C�� | 1mol����������7mol H2�����ӳɷ�Ӧ | |
| D�� | ����������FeCl3��Һ������ɫ��Ӧ |
CH3OH ��l��+$\frac{3}{2}$ O2��g��=CO2��g��+2H2O��l����H=-726.5KJ/mol��
��2���ӻ�ѧ���ĽǶȷ�������ѧ��Ӧ�Ĺ��̾��Ƿ�Ӧ��Ļ�ѧ�����ƻ���������Ļ�ѧ�����γɹ��̣���֪��Ӧ��N2��g��+3H2��g��?2NH3��g����H=a kJ•mol-1���йؼ������������
| ��ѧ�� | H-H | N-H | N��N |
| ���ܣ�kJ•mol-1�� | 436 | 391 | 945 |
��3�����ݸ�˹���ɿ��Զ�ijЩ����ͨ��ʵ��ֱ�Ӳⶨ�Ļ�ѧ��Ӧ�ķ�Ӧ�Ƚ������㣮��֪��
C��s��ʯī��+O2��g���TCO2��g����H1=-393.5kJ•mol-1
2H2��g��+O2��g���T2H2O��l����H2=-571.6kJ•mol-1
2C2H2��g��+5O2��g���T4CO2��g��+2H2O��l����H3=-2599kJ•mol-1
���ݸ�˹���ɣ�����298Kʱ��C��s��ʯī����H2��g������1mol C2H2��g����Ӧ�ķ�Ӧ��Ϊ��
��H=+226.7 KJ/mol��
��4�����������õ������£�NH4+����������Ӧ��������NO3-��������Ӧ�������仯ʾ
��ͼ��ͼ��

��һ����Ӧ�Ƿ��ȷ�Ӧ������ȡ������ȡ�����ԭ���Ƿ�Ӧ��������������������������
| A�� | 10mL0.1mol/L��AlCl3��Һ | B�� | 20mL0.2mol/L��CaCl2��Һ | ||
| C�� | 30mL0.2mol/L��KCl��Һ | D�� | 10mL0.25mol/L��NaCl��Һ |


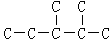 ����������һ�������6�֣�����������Ȳ�������Ƶã����Ȳ���Ľṹ��ʽΪ��CH3��2CH��CH3��CHC��CH
����������һ�������6�֣�����������Ȳ�������Ƶã����Ȳ���Ľṹ��ʽΪ��CH3��2CH��CH3��CHC��CH