题目内容
16.下列说法正确的是( )| A. | 丙烷没有同分异构体 | |
| B. | CH(CH3)2CH2CH2CH3的一氯代物有4种 | |
| C. | 二氯苯有3种,则四氯苯有6种 | |
| D. | CH3OH与CH2OH-CH2OH都属于醇,互为同系物 |
分析 A、丙烷只有一种结构为CH3CH2CH3;
B、根据分子中等效H原子判断,分子中由几种H原子,其一氯代物就有几种异构体;
C、若将二氯苯的氢原子换成四氯苯的氯原子,将二氯苯的氯原子换成四氯苯的氢原子,这在算同分异构体时是等效的,即二氯苯有多少同分异构体,那么四氯苯就有多少同分异构体;
D、同系物指结构相似、通式相同,组成上相差1个或者若干个CH2原子团,具有相同种类、数目的官能团的化合物.
解答 解:A、丙烷只有一种结构为CH3CH2CH3,不存在同分异构体,故A选;
B、CH(CH3)2CH2CH2CH3中有5种H原子,其一氯代物有5种,故B不选;
C、二氯苯的同分异构体有3种,二氯苯有多少同分异构体,四氯苯就有多少同分异构体,则四氯苯同分异构体的数目3种,故C不选;
D、CH3OH与CH2OH-CH2OH中含有羟基的数目不同,不是同系物,故C不选;
故选A.
点评 本题考查同分异构体、同系物的判断,难度不大,掌握判断的方法即可解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.已知:2Fe2++Br2=2Fe3++2Br-,2Br-+Cl2=Br2+2Cl-.现向含有amolFeBr2的溶液中,通入xmolCl2.下列各项为通入Cl2过程中,溶液中所发生反应的离子方程式,其中不正确的是( )
| A. | x=0.4a,2Fe2++Cl2=2Fe3++2Cl- | |
| B. | x=1.5a,2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl- | |
| C. | x=a,2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl- | |
| D. | x=0.6a,2Br-+Cl2=Br2+2Cl- |
4.金属的熔沸点与金属键强弱有关,判断下列金属熔点逐渐升高的是( )
| A. | Li、Na、K | B. | Na、Mg、Al | C. | Li、Be、Mg | D. | Li、Na、Mg |
11.既可以鉴别乙烷和乙炔,又可以除去乙烷中含有的乙炔的方法是( )
| A. | 足量的溴的四氯化碳溶液 | B. | 与足量的液溴反应 | ||
| C. | 点燃 | D. | 在一定条件下与氢气加成 |
1.等物质的量浓度的下列稀溶液:①乙醇、②苯酚、③碳酸、④乙酸,它们的pH由大到小排列正确的是( )
| A. | ①②③④ | B. | ③①②④ | C. | ④②③① | D. | ①③②④ |
6.汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体CO2和N2等.
(1)汽车尾气中CO、NO2气体在一定条件下可以发生反应:
4CO(g)+2NO2(g)?4CO2(g)+N2(g)△H=-1200kJ•mol-1.恒温恒容条件下,不能说明该反应已达到平衡状态的是CD(填序号);
A.容器内混合气体颜色不再变化 B.容器内的压强保持不变
C.2v逆(NO2)=v正(N2) D.容器内混合气体密度保持不变
对于该反应,温度不同(T2>T1)、其他条件相同时,下列图象正确的是乙(填代号).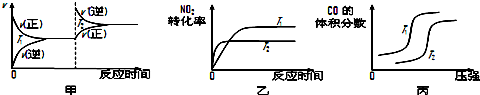
汽车尾气中CO与H2O(g)在一定条件下可以发生反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H<0; 某温度时在甲、乙、丙三个恒容密闭容器中,起始时按照右表进行投料,达到平衡状态时K=81.
(2)平衡时,甲容器中CO的转化率是90%;平衡时,比较容器中H2O的转化率:乙<甲(填“>”、“<”或“=”,下同);丙=甲.
(3)已知温度为T时:CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=+165KJ•mol
CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41KJ•mol.贮氢合金ThNi5可催化由CO、H2合成CH4的反应,温度为T时,该反应的热化学方程式是CO(g)+3H2(g)=CH4(g)+H2O(g)△H=-206kJ•mol?1.
(1)汽车尾气中CO、NO2气体在一定条件下可以发生反应:
4CO(g)+2NO2(g)?4CO2(g)+N2(g)△H=-1200kJ•mol-1.恒温恒容条件下,不能说明该反应已达到平衡状态的是CD(填序号);
A.容器内混合气体颜色不再变化 B.容器内的压强保持不变
C.2v逆(NO2)=v正(N2) D.容器内混合气体密度保持不变
对于该反应,温度不同(T2>T1)、其他条件相同时,下列图象正确的是乙(填代号).

汽车尾气中CO与H2O(g)在一定条件下可以发生反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H<0; 某温度时在甲、乙、丙三个恒容密闭容器中,起始时按照右表进行投料,达到平衡状态时K=81.
| 起始物质的量 | 甲 | 乙 | 丙 |
| n(H2O)/mol | 0.10 | 0.20 | 0.20 |
| n(CO)/mol | 0.10 | 0.10 | 0.20 |
(3)已知温度为T时:CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=+165KJ•mol
CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41KJ•mol.贮氢合金ThNi5可催化由CO、H2合成CH4的反应,温度为T时,该反应的热化学方程式是CO(g)+3H2(g)=CH4(g)+H2O(g)△H=-206kJ•mol?1.
7.三个密闭容器中分别充入H2、O2、CO2三种气体,以下各种情况下排序正确的是( )
| A. | 当它们的压强和体积、温度均相同时,三种气体的质量:m(H2)>m(O2)>m(CO2) | |
| B. | 当它们的温度和压强均相同时,三种气体的密度:ρ(H2)>ρ(02)>ρ(C02) | |
| C. | 当它们的质量和温度、压强均相同时,三种气体的体积:V(CO2)>V(O2)>V(H2) | |
| D. | 当它们的温度和密度都相同时,三种气体的压强:P(H2)>P(O2)>P(CO2) |
 .
.