题目内容
下列说法正确的是( )
| A、酯化反应、硝化反应以及酯的水解均属于取代反应类型 |
| B、乙醇生成溴乙烷和乙烯生成溴乙烷的反应类型相同 |
| C、可用氢氧化钠溶液除去乙酸乙酯中混有乙酸和乙醇 |
| D、蛋白质、淀粉、油脂均属于天然高分子化合物,均能发生水解反应 |
考点:取代反应与加成反应,有机高分子化合物的结构和性质,物质的分离、提纯和除杂
专题:
分析:A、酯化反应、硝化反应以及酯的水解反应均属于取代反应;
B、乙醇生成溴乙烷是取代反应,乙烯生成溴乙烷是加成反应;
C、氢氧化钠能使乙酸乙酯水解;
D、油脂属于小分子化合物.
B、乙醇生成溴乙烷是取代反应,乙烯生成溴乙烷是加成反应;
C、氢氧化钠能使乙酸乙酯水解;
D、油脂属于小分子化合物.
解答:
解:A、酯化反应、硝化反应以及酯的水解反应均属于取代反应,正确;
B、乙醇生成溴乙烷是取代反应,乙烯生成溴乙烷是加成反应,故两者反应类型不同,故错误;
C、氢氧化钠能使乙酸乙酯水解,所以不能用氢氧化钠作除杂剂,应选取饱和碳酸钠溶液作除杂剂,故错误;
D、油脂属于小分子化合物,但油脂能发生水解反应,故D错误,故选A.
B、乙醇生成溴乙烷是取代反应,乙烯生成溴乙烷是加成反应,故两者反应类型不同,故错误;
C、氢氧化钠能使乙酸乙酯水解,所以不能用氢氧化钠作除杂剂,应选取饱和碳酸钠溶液作除杂剂,故错误;
D、油脂属于小分子化合物,但油脂能发生水解反应,故D错误,故选A.
点评:本题考查了有机物的反应类型、结构和性质,较基础,熟悉常见有机物的结构和性质是解题的基础.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
下列化学用语的表达或使用正确的是( )
A、氟离子的结构示意图: |
B、CH4的比例模型: |
C、羧基的电子式: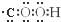 |
| D、NaHCO3的电离方程式:NaHCO3═Na++H++CO32- |
下列有关物质性质的说法错误的是( )
| A、热稳定性:HCl>HBr>HI |
| B、原子半径:Na>Mg>Al |
| C、还原性:PH3>H2S>HCl |
| D、结合质子能力:ClO->HCO3->SiO32- |
下列化学方程式或离子方程式中,正确的是( )
A、用浓硫酸与4-溴-1-丁醇加热发生消去反应:BrCH2CH2CH2OH
| |||
B、水杨酸( )中加入NaHCO3溶液: )中加入NaHCO3溶液: +2HCO3→ +2HCO3→ +2CO2↑+2H2O +2CO2↑+2H2O | |||
| C、在氢氧化钡溶液中滴加硫酸氢钾溶液至pH=7:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |||
| D、用侯氏制碱法制得NaHCO3:Na++NH3+CO2+H2O=NaHCO3↓+NH4+ |
下列有关事实的叙述正确的是( )
| A、电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属 |
| B、玻璃钢、航天飞机上的隔热陶瓷瓦都属于复合材料 |
| C、氧化钠可作为呼吸面具和潜水艇里氧气的来源 |
| D、铝-空气燃料电池通常以NaOH溶液为电解液,电池在工作过程中电解液的pH保持不变 |
 )在一定条件下可以发生如下图所示的转化(其他产物和水已略去).
)在一定条件下可以发生如下图所示的转化(其他产物和水已略去).
 )经过几步有机反应制得,其中最佳的次序是:
)经过几步有机反应制得,其中最佳的次序是:

 随着能源与环境问题越来越被人们关注,碳一化学(C1化学)成为研究的热点.“碳一化学”即以单质碳及CO、CO2、CH4、CH3OH等含一个碳原子的物质为原料合成工业产品的化学与工艺.
随着能源与环境问题越来越被人们关注,碳一化学(C1化学)成为研究的热点.“碳一化学”即以单质碳及CO、CO2、CH4、CH3OH等含一个碳原子的物质为原料合成工业产品的化学与工艺.