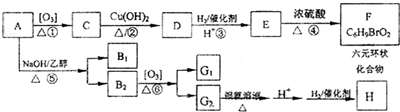
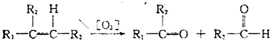题目内容
下列有关物质性质的说法错误的是( )
| A、热稳定性:HCl>HBr>HI |
| B、原子半径:Na>Mg>Al |
| C、还原性:PH3>H2S>HCl |
| D、结合质子能力:ClO->HCO3->SiO32- |
考点:元素周期律的作用
专题:元素周期律与元素周期表专题
分析:A、非金属的氢化物稳定性和非金属性一致,氢化物越稳定非金属性越强,同主族从上到下非金属性减弱;
B、电子层数相同核电荷数越多半径越小;
C、元素的非金属性越强,对应的单质的氧化性越强,其氢化物的还原性越弱;
D、酸性越弱,酸越难电离,对应的酸根离子越易结合氢离子.
B、电子层数相同核电荷数越多半径越小;
C、元素的非金属性越强,对应的单质的氧化性越强,其氢化物的还原性越弱;
D、酸性越弱,酸越难电离,对应的酸根离子越易结合氢离子.
解答:
解:A、氢化物越稳定非金属性越强,同主族从上到下非金属性减弱,热稳定性:HI<HBr<HCl,故A正确;
B、电子层数相同核电荷数越多半径越小,所以原子半径:Na>Mg>Al,故B正确;
C、元素的非金属性:P<S<Cl,元素的非金属性越强,对应的单质的氧化性越强,其氢化物的还原性越弱,所以还原性:PH3>H2S>HCl,故C正确;
D、酸性越弱,酸越难电离,对应的酸根离子越易结合氢离子,碳酸的酸性大于次氯酸,强于硅酸,所以结合质子的能力:SiO32->ClO->HCO3-,故D错误;
故选D.
B、电子层数相同核电荷数越多半径越小,所以原子半径:Na>Mg>Al,故B正确;
C、元素的非金属性:P<S<Cl,元素的非金属性越强,对应的单质的氧化性越强,其氢化物的还原性越弱,所以还原性:PH3>H2S>HCl,故C正确;
D、酸性越弱,酸越难电离,对应的酸根离子越易结合氢离子,碳酸的酸性大于次氯酸,强于硅酸,所以结合质子的能力:SiO32->ClO->HCO3-,故D错误;
故选D.
点评:本题考查元素的金属性、非金属性的递变规律,半径比较,酸性的比较,题目难度中等.

练习册系列答案
相关题目
下列金属中,既属于有色金属又属于轻金属的是( )
| A、铁 | B、铬 | C、钠 | D、银 |
下列说法正确的是( )
| A、酯化反应、硝化反应以及酯的水解均属于取代反应类型 |
| B、乙醇生成溴乙烷和乙烯生成溴乙烷的反应类型相同 |
| C、可用氢氧化钠溶液除去乙酸乙酯中混有乙酸和乙醇 |
| D、蛋白质、淀粉、油脂均属于天然高分子化合物,均能发生水解反应 |
对于平衡CO2(g)?CO2(aq)△H=-19.75kJ?mol-1,为增大二氧化碳气体在水中的溶解度,应采用的方法是( )
| A、升温增压 | B、降温减压 |
| C、升温减压 | D、降温增压 |
某同学组装了如图所示的电化学装置.电极I为Al,其他电极均为Cu,则( )


| A、工作一段时间后,C烧杯的PH减小 |
| B、电极I发生还原反应 |
| C、盐桥中的K+移向A烧杯 |
D、电流方向:电极Ⅳ→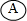 →电极I →电极I |
《实验化学》教材在教材结构、实验课题编排和内容选择等方面都作了精心设计.下列结论均出自《实验化学》中的实验,其中错误的是( )
| A、食醋用氢氧化钠溶液滴定开始时,溶液的pH通常变化缓慢,当接近完全反应时(即滴定终点),pH出现突变,称为滴定突跃 |
| B、当锌完全溶解后,铁与酸反应产生氢气的速率会显著减慢,此现象可作为判断镀锌铁皮中锌镀层是否完全被反应掉的依据 |
| C、油墨是由多种色素按一定比例混合而成的,某同学欲用纸层析的方法将其主要色素分离开来,可选用的展开剂的物质是丙酮和盐酸 |
| D、提取海带中碘元素时,为保证I-完全氧化为I2,加入的氧化剂(H2O2或新制氯水)均应过量 |