题目内容
19.下列离子方程式书写正确的是( )| A. | 铜片与浓硫酸加热反应:Cu+4H++SO42-$\frac{\underline{\;\;△\;\;}}{\;}$ Cu2++SO2↑+2H2O | |
| B. | 向漂白精溶液中通入少量CO2:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO | |
| C. | H2C2O4溶液能使KMnO4酸性溶液褪色 2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O | |
| D. | 向Fe(NO3)2溶液中加入过量的HI溶液 3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
分析 A.浓硫酸在离子反应中保留化学式;
B.反应生成碳酸钙、HClO;
C.发生氧化还原反应,遵循电子、电荷守恒,醋酸在离子反应中保留化学式;
D.碘化氢过量,铁离子和硝酸根离子都完全反应,漏掉了硝酸根离子与碘离子的反应.
解答 解:A.铜片与浓硫酸加热反应:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ Cu2++SO42-+SO2↑+2H2O,故A错误;
B.向漂白精溶液中通入少量CO2的离子反应为Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO,故B正确;
C.H2C2O4溶液能使KMnO4酸性溶液褪色的离子反应为2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O,故C错误
D.硝酸铁溶液中滴加足量HI溶液,铁离子和硝酸根离子都参与反应,正确的离子方程式为:Fe3++3NO3-+12H++10I-=Fe2++5I2+3NO↑+6H2O,故D错误;
故选B.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应方程式的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案
相关题目
9.含氮废水在排入水体之前需进行脱氮处理以减缓水体富营养化.某化肥厂废水中NH4+的浓度为54mg/L,在微生物作用的条件下脱氮处理:
①NH4++O2-NO2-+H++H2O(未配平)
②2NO2-+O2=2NO3-
③6NO3-+5CH3OH+6H+=3N2+5X+13H2O
下列说法中正确的是( )
①NH4++O2-NO2-+H++H2O(未配平)
②2NO2-+O2=2NO3-
③6NO3-+5CH3OH+6H+=3N2+5X+13H2O
下列说法中正确的是( )
| A. | 反应①配平后,H2O的化学计量数为4 | |
| B. | 若反应②有2mol电子发生转移,则生成1molNO3- | |
| C. | 反应③中生成物X为CO32- | |
| D. | 1L废水完全脱氮所需CH3OH的质量为0.08g |
4.下列离子方程式正确的是( )
| A. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═[Al(OH)4]-+4NH4+ | |
| B. | MgSO4溶液中加入Ba(OH)2溶液:SO42-+Ba2+═BaSO4↓ | |
| C. | NaHCO3溶液加入少量Ca(OH)2溶液:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| D. | 硫化钠溶液显碱性:S2-+2H2O?H2S+2OH- |
11.鸡蛋壳的主要成分是碳酸钙,碳酸钙中钙的质量分数是( )
| A. | 25% | B. | 40% | C. | 50% | D. | 60% |
8.下列物质中,不能作为食品添加剂的是( )
| A. | 白醋 | B. | 白酒 | C. | 甲醇 | D. | 食盐 |
2.分子式与苯丙氨酸( )相同,且同时符合下列条件:①有带两个取代基的苯环,②有一个硝基直接连接在苯环上,这种同分异构体的数目为( )
)相同,且同时符合下列条件:①有带两个取代基的苯环,②有一个硝基直接连接在苯环上,这种同分异构体的数目为( )
 )相同,且同时符合下列条件:①有带两个取代基的苯环,②有一个硝基直接连接在苯环上,这种同分异构体的数目为( )
)相同,且同时符合下列条件:①有带两个取代基的苯环,②有一个硝基直接连接在苯环上,这种同分异构体的数目为( )| A. | 3种 | B. | 6种 | C. | 8种 | D. | 10种 |
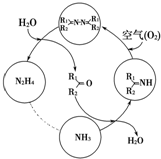 利用空气催化氧化法制取联氨,其有关物质的转化如图所示(R1、R2代表烃基).
利用空气催化氧化法制取联氨,其有关物质的转化如图所示(R1、R2代表烃基). .
.