题目内容
小明很喜欢化学实验课,今天要学习“探究铁及其化合物的氧化性或还原性”.
(1)实验前小明预测说:Fe2+肯定既有还原性又有氧化性.你认为他预测的依据是: .
(2)小明欲用实验证明他的预测.实验室提供了下列试剂:3%的H2O2溶液、锌粒、铜片、0.1mol?L-1FeCl2溶液、KSCN溶液、新制氯水.
①若小明计划在0.1mol?L-1FeCl2溶液滴入新制氯水,探究Fe2+的还原性,你预计可能发生的反应是: (写离子方程式),可能观察到的现象是:溶液由浅绿色变为 色.
②实验中,小明发现现象不太明显,老师分析可能是产物的含量太低,建议可以通过检验Fe2+被氧化的产物Fe3+的存在以获取证据.你认为可选 滴入小明所得的混合液中,并通过溶液出现 色的现象,证明小明的观点和实验方案都是正确的.
③对于证明Fe2+具有氧化性,小明认为金属单质都具有还原性,并分别将铜片、锌粒投入FeCl2溶液中,结果铜片没变化,锌粒逐渐变小.由此说明三种金属的还原性由强至弱的顺序为: .
④实际上Fe2+的还原性较强,实验室的FeCl2溶液常因氧化而变质.除杂的方法是:加入 ,相关反应的离子方程式: .
(1)实验前小明预测说:Fe2+肯定既有还原性又有氧化性.你认为他预测的依据是:
(2)小明欲用实验证明他的预测.实验室提供了下列试剂:3%的H2O2溶液、锌粒、铜片、0.1mol?L-1FeCl2溶液、KSCN溶液、新制氯水.
①若小明计划在0.1mol?L-1FeCl2溶液滴入新制氯水,探究Fe2+的还原性,你预计可能发生的反应是:
②实验中,小明发现现象不太明显,老师分析可能是产物的含量太低,建议可以通过检验Fe2+被氧化的产物Fe3+的存在以获取证据.你认为可选
③对于证明Fe2+具有氧化性,小明认为金属单质都具有还原性,并分别将铜片、锌粒投入FeCl2溶液中,结果铜片没变化,锌粒逐渐变小.由此说明三种金属的还原性由强至弱的顺序为:
④实际上Fe2+的还原性较强,实验室的FeCl2溶液常因氧化而变质.除杂的方法是:加入
考点:性质实验方案的设计
专题:
分析:(1)依据元素化合价分析物质具有的氧化性还原性判断,元素化合价最高价具有氧化性,最低价具有还原性,据中间价态既具有氧化性又具有还原性;
(2)①在0.1mol?L-1FeCl2溶液滴入新制氯水,探究Fe2+的还原性,依据氯水中的氯气具有强氧化性能氧化亚铁离子,溶液由浅绿色变为黄色;
②验证三价铁离子的方法是硫氰酸钾溶液遇铁离子变血红色判断;
③氧化还原反应中还原剂的还原性大于还原产物分析判断;
④防止亚铁盐溶液被氧化,需要加入铁粉;
(2)①在0.1mol?L-1FeCl2溶液滴入新制氯水,探究Fe2+的还原性,依据氯水中的氯气具有强氧化性能氧化亚铁离子,溶液由浅绿色变为黄色;
②验证三价铁离子的方法是硫氰酸钾溶液遇铁离子变血红色判断;
③氧化还原反应中还原剂的还原性大于还原产物分析判断;
④防止亚铁盐溶液被氧化,需要加入铁粉;
解答:
解:(1)元素化合价处于最高价只具有氧化性,处于最低价只具有还原性,处于中间价态既可以升高也可以降低,既具有氧化性又具有还原性;
故答案为:因为Fe2+中铁元素化合价处于中间价态,可以升高也可以降低;
(2)①在0.1mol?L-1FeCl2溶液滴入新制氯水,氯气具有强氧化性能源和亚铁离子为铁离子,反应的离子方程式为:Cl2+2Fe2+=2Cl-+2Fe3+;
溶液颜色从浅绿色变为黄色;
故答案为:Cl2+2Fe2+=2Cl-+2Fe3+;黄;
②通过检验Fe2+被氧化的产物Fe3+的存在以获取证据.需要的试剂为硫氰酸钾溶液,发生反应,Fe3++3SCN-=Fe(SCN)3,溶液变血红色,
故答案为:硫氰酸钾溶液;血红;
③金属单质都具有还原性,分别将铜片、锌粒投入FeCl2溶液中,结果铜片没变化,锌粒逐渐变小,发生反应Zn+Fe2+=Fe+Zn2+;氧化还原反应中还原剂的还原性大于还原产物,锌的还原性大于铁,铁大于铜,故答案为:Zn Fe Cu;
④实验室的FeCl2溶液常因氧化而变质,为防止亚铁离子的氧化,需要加入还原铁粉,发生反应2Fe3++Fe=3Fe2+;避免亚铁离子的氧化,
故答案为:加入适量铁粉,2Fe3++Fe=3Fe2+.
故答案为:因为Fe2+中铁元素化合价处于中间价态,可以升高也可以降低;
(2)①在0.1mol?L-1FeCl2溶液滴入新制氯水,氯气具有强氧化性能源和亚铁离子为铁离子,反应的离子方程式为:Cl2+2Fe2+=2Cl-+2Fe3+;
溶液颜色从浅绿色变为黄色;
故答案为:Cl2+2Fe2+=2Cl-+2Fe3+;黄;
②通过检验Fe2+被氧化的产物Fe3+的存在以获取证据.需要的试剂为硫氰酸钾溶液,发生反应,Fe3++3SCN-=Fe(SCN)3,溶液变血红色,
故答案为:硫氰酸钾溶液;血红;
③金属单质都具有还原性,分别将铜片、锌粒投入FeCl2溶液中,结果铜片没变化,锌粒逐渐变小,发生反应Zn+Fe2+=Fe+Zn2+;氧化还原反应中还原剂的还原性大于还原产物,锌的还原性大于铁,铁大于铜,故答案为:Zn Fe Cu;
④实验室的FeCl2溶液常因氧化而变质,为防止亚铁离子的氧化,需要加入还原铁粉,发生反应2Fe3++Fe=3Fe2+;避免亚铁离子的氧化,
故答案为:加入适量铁粉,2Fe3++Fe=3Fe2+.
点评:本题考查了元素化合价变化与氧化性还原性的关系判断,铁及其化合物性质的应用,离子检验的方法应用,氧化还原反应概念的分析判断,题目较简单.

练习册系列答案
相关题目
在一固定容积的密闭容器中进行如下反应:N2+3H2?2NH3 △H<O,在一定温度下反应达到平衡状态,若将平衡体系中各物质的浓度都增加到原来的2倍,下列叙述正确的是( )
| A、化学平衡不发生移动 |
| B、化学平衡向正反应方向移动 |
| C、化学平衡向逆反应方向移动 |
| D、正反应速率增大,逆反应速率减小 |
下列实验过程中,始终无明显现象的是( )
| A、NH3通入FeSO4溶液中 |
| B、CO2通入CaCl2溶液中 |
| C、AlCl3溶液中滴入NaHCO3溶液 |
| D、SO2通入Ba(NO3)2溶液中 |
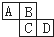 如图为周期表中的一部分.已知A、B、C、D均为短周期元素,A与D原子序数之和为C原子序数的1.5倍.
如图为周期表中的一部分.已知A、B、C、D均为短周期元素,A与D原子序数之和为C原子序数的1.5倍. 某研究性学习小组设计实验方案来研究稀硝酸与铜反应生成NO.
某研究性学习小组设计实验方案来研究稀硝酸与铜反应生成NO.