题目内容
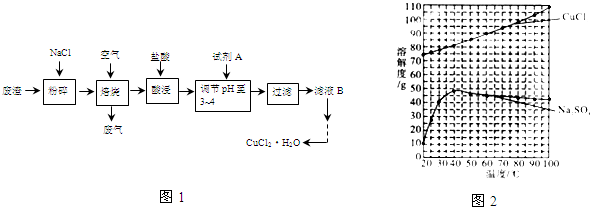
某炼铁废渣中含有大量CuS及少量铁的化合物,工业上以该废渣为原料生产CuCl2?2H2O的工艺流程如图1:
回答下列问题:
(1)配平并完成化学方程式.焙烧过程中发生的主要反应为:
CuS+ + O2
CuCl2+ Na2SO4
(2)试剂A应选用 (填编号),理由是 .
①NaClO ②Cl2③H2O2溶液④浓硫酸
(3)过滤操作中除滤纸、玻璃棒外,还要用到的玻璃仪器有 ;滤液B中大量含有的离子有 .
(4)为了获得CuCl2?H2O晶体,对滤液B进行的操作是: ,趁热过滤,过滤得到产品.分析有关物质的溶解度曲线(如图2),“趁热过滤”得到的固体是 ,析出CuCl2?H2O晶体的合适温度为 .

回答下列问题:
(1)配平并完成化学方程式.焙烧过程中发生的主要反应为:
| ||
(2)试剂A应选用
①NaClO ②Cl2③H2O2溶液④浓硫酸
(3)过滤操作中除滤纸、玻璃棒外,还要用到的玻璃仪器有
(4)为了获得CuCl2?H2O晶体,对滤液B进行的操作是:
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:流程分析废渣粉碎加入氯化钠,通入空气焙烧后加入盐酸酸浸,加入试剂A是氧化剂将亚铁离子氧化为铁离子,调节溶液PH使铁离子沉淀;过滤后的滤液中主要是氯化铜溶液蒸发浓缩,冷却结晶得到氯化铜晶体;
(1)利用化合价升降相等配出氧化剂和还原剂的化学计量数,然后根据原子守恒把其他物质配平;
(2)试剂A满足能把亚铁离子氧化为铁离子和调节PH使酸性减弱两个功能;
(3)经过盐酸酸浸,NaClO调节PH值,过滤掉氢氧化铁后,溶液中还有Cu2+、Na+、Cl-、SO42-;
(4)蒸发浓缩后,由于同温下硫酸钠的溶解度小,会有大量硫酸钠析出;
40摄氏度时硫酸钠溶解度最大,硫酸钠最不容易析出,为了得到更多的析出CuCl2?2H2O晶体,温度略低于40℃的范围.
(1)利用化合价升降相等配出氧化剂和还原剂的化学计量数,然后根据原子守恒把其他物质配平;
(2)试剂A满足能把亚铁离子氧化为铁离子和调节PH使酸性减弱两个功能;
(3)经过盐酸酸浸,NaClO调节PH值,过滤掉氢氧化铁后,溶液中还有Cu2+、Na+、Cl-、SO42-;
(4)蒸发浓缩后,由于同温下硫酸钠的溶解度小,会有大量硫酸钠析出;
40摄氏度时硫酸钠溶解度最大,硫酸钠最不容易析出,为了得到更多的析出CuCl2?2H2O晶体,温度略低于40℃的范围.
解答:
解:(1)CuS→Na2SO4 S化合价升高8,O2→Na2SO4 O化合价降低2,O2化合价降低2×2=4,根据化合价升降相等可得,CuS化学计量数为1,氧气的化学计量数为2,根据元素守恒Na2SO4化学计量数为1,NaCl化学计量数为2,CuCl2化学计量数为1,配平化学方程式为CuS+2NaCl+2O2
CuCl2+Na2SO4;
故答案为:1;2NaCl;2;1;1;
(2)NaClO、Cl2、H2O2溶液、浓硫酸均能将Fe2+氧化为Fe3+,但氯水和硫酸溶液均呈酸性,NaClO溶液呈碱性,故可以起到调节PH的作用,
故答案为:①;NaClO能将Fe2+氧化为Fe3+,且溶液显碱性,能增大溶液pH使Fe3+沉淀;
(3)过滤操作中除滤纸、玻璃棒外,还要用到的玻璃仪器有烧杯和漏斗;经过盐酸酸浸,NaClO调节PH值,过滤掉氢氧化铁后,溶液中还有Cu2+、Na+、Cl-、SO42-;
故答案为:烧杯、漏斗;Cu2+、Na+、Cl-、SO42-;
(4)由图乙可知硫酸钠的溶解度较小而且温度较高时随温度的变化不大,为了防止氯化铜晶体的析出,必须趁热过滤,加热浓缩时会有大量的硫酸钠析出;冷却结晶时尽量保证硫酸钠不析出,而40摄氏度时硫酸钠溶解度最大,为了能析出更多的CuCl2?2H2O晶体,故适宜温度为35~40℃.
故答案为:蒸发浓缩,冷却结晶;Na2SO4;30~35℃.
| ||
故答案为:1;2NaCl;2;1;1;
(2)NaClO、Cl2、H2O2溶液、浓硫酸均能将Fe2+氧化为Fe3+,但氯水和硫酸溶液均呈酸性,NaClO溶液呈碱性,故可以起到调节PH的作用,
故答案为:①;NaClO能将Fe2+氧化为Fe3+,且溶液显碱性,能增大溶液pH使Fe3+沉淀;
(3)过滤操作中除滤纸、玻璃棒外,还要用到的玻璃仪器有烧杯和漏斗;经过盐酸酸浸,NaClO调节PH值,过滤掉氢氧化铁后,溶液中还有Cu2+、Na+、Cl-、SO42-;
故答案为:烧杯、漏斗;Cu2+、Na+、Cl-、SO42-;
(4)由图乙可知硫酸钠的溶解度较小而且温度较高时随温度的变化不大,为了防止氯化铜晶体的析出,必须趁热过滤,加热浓缩时会有大量的硫酸钠析出;冷却结晶时尽量保证硫酸钠不析出,而40摄氏度时硫酸钠溶解度最大,为了能析出更多的CuCl2?2H2O晶体,故适宜温度为35~40℃.
故答案为:蒸发浓缩,冷却结晶;Na2SO4;30~35℃.
点评:本题考查了物质的分离和提纯、离子的检验及沉淀溶解平衡,难度中等.注意除杂不能引入新的杂质,重结晶法提纯物质温度的选择是易出错点.

练习册系列答案
相关题目
下列反应中生成物的总能量大于反应物总能量的是( )
| A、氢气在氧气中燃烧 |
| B、铁丝在氧气中燃烧 |
| C、硫在氧气中燃烧 |
| D、焦炭在高温下与水蒸气反应 |
用胆矾(CuSO4?5H2O)晶体配制0.1mol/L的CuSO4溶液500mL,下列方法正确的是( )
| A、称取8.0g胆矾使其溶于500mL水中 |
| B、称取12.5g胆矾使其溶于500mL水中 |
| C、称取12.5g胆矾使其溶于适量水中,再加水稀释至500mL. |
| D、称取8.0g胆矾使其溶于375g水中 |