题目内容
下列实验过程中,始终无明显现象的是( )
| A、NH3通入FeSO4溶液中 |
| B、CO2通入CaCl2溶液中 |
| C、AlCl3溶液中滴入NaHCO3溶液 |
| D、SO2通入Ba(NO3)2溶液中 |
考点:二氧化硫的化学性质,氨的化学性质
专题:
分析:A.一水合氨与硫酸亚铁反应生成氢氧化亚铁;
B.碳酸的酸性弱于盐酸;
C.AlCl3溶液中滴入NaHCO3溶液,发生双水解,生成氢氧化铝和二氧化碳;
D.二氧化硫与水反应生成亚硫酸,能够被硝酸根氧化生成硫酸根离子,硫酸根与钡离子反应生成硫酸钡沉淀.
B.碳酸的酸性弱于盐酸;
C.AlCl3溶液中滴入NaHCO3溶液,发生双水解,生成氢氧化铝和二氧化碳;
D.二氧化硫与水反应生成亚硫酸,能够被硝酸根氧化生成硫酸根离子,硫酸根与钡离子反应生成硫酸钡沉淀.
解答:
解:A.NH3通入FeSO4溶液中,反应生成氢氧化亚铁白色沉淀,故A不选;
B.碳酸的酸性弱于盐酸,CO2通入CaCl2溶液中不发生反应,没有明显现象,故B选;
C.AlCl3溶液中滴入NaHCO3溶液发生双水解,生成氢氧化铝和二氧化碳,既有白色沉淀生成,又有气泡冒出,故 C不选;
D.SO2通入Ba(NO3)2溶液中,反应生成硫酸钡沉淀,故D不选;
故选:B.
B.碳酸的酸性弱于盐酸,CO2通入CaCl2溶液中不发生反应,没有明显现象,故B选;
C.AlCl3溶液中滴入NaHCO3溶液发生双水解,生成氢氧化铝和二氧化碳,既有白色沉淀生成,又有气泡冒出,故 C不选;
D.SO2通入Ba(NO3)2溶液中,反应生成硫酸钡沉淀,故D不选;
故选:B.
点评:本题考查了元素化合物的知识,明确物质的性质是解题关键,注意氯化铝与碳酸氢钠溶液发生的双水解反应,题目难度不大.

练习册系列答案
相关题目
工业生产中物质制备时,通过下列反应原理一步完成获得产物、符合“绿色化学”原则的反应是( )
| A、化合反应 | B、分解反应 |
| C、复分解反应 | D、置换反应 |
下图为向25ml0.1mol/LNaOH溶液中逐滴0.2mol/L醋酸溶液,曲线如下图所示,在AB区间,c(OH-)>c(H+),则c(OH-)与c(CH3COO-)大小关系是( )
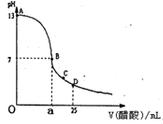

| A、c(OH-)一定大于c(CH3COO-) |
| B、c(OH-)一定小于c(CH3COO-) |
| C、c(OH-)一定等于c(CH3COO-) |
| D、上述三种情况都可能 |
用胆矾(CuSO4?5H2O)晶体配制0.1mol/L的CuSO4溶液500mL,下列方法正确的是( )
| A、称取8.0g胆矾使其溶于500mL水中 |
| B、称取12.5g胆矾使其溶于500mL水中 |
| C、称取12.5g胆矾使其溶于适量水中,再加水稀释至500mL. |
| D、称取8.0g胆矾使其溶于375g水中 |
下列实验中,(1)配制一定物质的量浓度的溶液(2)pH试纸的使用(3)过滤(4)蒸发,均需用到的仪器是( )
| A、试管 | B、容量瓶 |
| C、玻璃棒 | D、漏斗 |