题目内容
13.向明矾KAl(SO4)2.12H2O溶液里滴入Ba(OH)2溶液,当SO42-恰好完全沉淀时,其中元素的存在形式为( )| A. | 全部形成AlO2- | B. | 全都为Al(OH)3 | ||
| C. | 一部分为Al(OH)3,一部分为Al3+ | D. | 一部分为Al(OH)3,一部分为AlO2- |
分析 设明矾KAl(SO4)2•12H2O为1mol,则溶液中含有1molK+、1molAl3+、2molSO42-,根据反应:SO42-+Ba2+═BaSO4↓,当溶液中的SO42-完全沉淀时,需要2molBa2+,即2molBa(OH)2,2molBa(OH)2中含有4molOH-,1molAl3+和4molOH-发生反应:Al3++4OH-═AlO2-+2H2O,据此分析.
解答 解:设明矾KAl(SO4)2•12H2O为1mol,则溶液中含有1molK+、1molAl3+、2molSO42-,根据反应:SO42-+Ba2+═BaSO4↓,当溶液中的SO42-完全沉淀时,需要2molBa2+,即2molBa(OH)2,2molBa(OH)2中含有4molOH-,1molAl3+和4molOH-发生反应:Al3++4OH-═AlO2-+2H2O,铝元素的存在形式为:AlO2-.
故选A.
点评 本题考查了离子反应,注意判断使SO42-全部转化成BaSO4沉淀需要Ba(OH)2的物质的量,根据Al3+和OH-物质的量的关系判断反应产物,题目难度中等.

练习册系列答案
相关题目
1.一块表面已被氧化为Na2O的钠块10.8g,将其投入100g水中,产生H20.2g,则被氧化的钠是( )
| A. | 9.2g | B. | 10.6g | C. | 6.2g | D. | 4.6g |
8.某二元弱酸(H2A)溶液按下式发生一级电离和二级电离:H2AHA-+H+HA-A2-+H+下列溶液中C(A2-)最大的是( )
| A. | 0.01 mol•L-1的H2A溶液 | |
| B. | 0.01 mol•L-1NaHA溶液 | |
| C. | 0.02 mol•L-1HCl溶液与0.04 mol•L-1NaHA溶液等体积混合 | |
| D. | 0.02mol•L-1 NaOH溶液0.02 mol•L-1 NaHA溶液等体积混合 |
18.下列有关碳酸(H2CO3)和硅酸(H2SiO3)的说法中不正确的是( )
| A. | 两者均为弱酸 | |
| B. | 两者均可使紫色石蕊试液变红色 | |
| C. | CO2气体通入Na2SiO3溶液中可以制得硅酸 | |
| D. | 两者受热时均可以分解 |
5.常温下,一定量冰醋酸加水稀释过程中,溶液的导电性如下图所示.下列说法正确的是( )
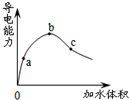

| A. | pH值:b>a>c | |
| B. | 与锌反应起始速率:a=b=c | |
| C. | 水电离的c(H+) c>a>b | |
| D. | 加入足量的NaHCO3固体,产生气体体积:a>b>c |
2.下列用来表示物质变化的化学用语中,错误的是( )
| A. | 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+ | |
| B. | 粗铜精炼时,与电源负极相连的是纯铜,电极反应式为:Cu2++2e-═Cu | |
| C. | 用Pt电极电解氯化铝溶液:2Cl-+2 H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2+2OH- | |
| D. | 由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+4OH-═AlO2-+2H2O |