题目内容
1.工业上以侯氏制碱法为基础生产焦亚硫酸钠(Na2S2O5).其制备工艺流程如下:
已知:反应Ⅱ包含2NaHSO3?Na2S2O5+H2O等多步反应.
(1)反应I的化学方程式为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl.
(2)“灼烧”时发生反应的化学方程式:2CuS+3O2$\frac{\underline{\;高温\;}}{\;}$2CuO+2SO2.
(3)已知Na2S2O5与稀硫酸反应放出SO2,其离子方程式为:S2O52-+2H+=2SO2↑+H2O.
(4)反应I时应先通的气体为NH3副产品X的化学式是CuSO4•5H2O.生产中可循环利用的物质为CO2(填化学式)
(5)为了减少产品Na2S2O5中杂质含量,需控制反应Ⅱ中气体与固体的物质的量之比约为2:1.检验产品中含有碳酸钠杂质所需试剂是①③⑥(填编号)
①酸性高锰酸钾 ②品红溶液 ③澄清石灰水
④饱和碳酸氢钠溶液 ⑤NaOH ⑥稀硫酸.
分析 反应Ⅰ为生成NaHCO3,加热生成Na2CO3,在反应Ⅱ中二氧化硫与碳酸钠反应生成NaHSO3与二氧化碳,加热NaHSO3生成Na2S2O5,
(1)根据流程确定反应物为NaCl、NH3、CO2,产物为NH4Cl和碳酸氢钠;
(2)CuS与氧气反应生成黑色氧化铜和二氧化硫气体,根据化学方程式可计算出转移电子的物质的量;
(3)Na2S2O5中硫元素的化合价为+4价,生成二氧化硫化合价没变;
(4)反应Ⅰ进行时应先通入氨气,增大HCO3-的浓度,便于NaHCO3析出;氧化铜与硫酸反应生成硫酸铜,结晶得出硫酸铜晶体;根据流程图可知,可循环使用的物质是二氧化碳;
(5)反应Ⅱ中反应应是二氧化硫与碳酸钠反应生成NaHSO3,NaHSO3再生成Na2S2O5,反应方程式为Na2CO3+2 SO2+H2O=2NaHSO3+CO2,为了控制杂质,二氧化硫与碳酸氢钠应按反应方程式中比例关系反应;检验产品中含有碳酸钠杂质,需加酸反应检验二氧化碳生成,即用的澄清石灰水,但加酸会生成二氧化硫,二氧化硫也能使澄清石灰水变浑浊,故应先除去,用酸性高锰酸钾溶液根据颜色不褪色确定二氧化硫除净,据此答题.
解答 解:(1)流程确定反应物为NaCl、NH3、CO2,产物为NH4Cl和碳酸氢钠,反应Ⅰ的化学方程式为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,
故答案为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl;
(2)硫化铜灼烧一定生成氧化铜和二氧化硫,反应的化学方程式为:2CuS+3O2$\frac{\underline{\;高温\;}}{\;}$2CuO+2SO2,故答案为:2CuS+3O2$\frac{\underline{\;高温\;}}{\;}$2CuO+2SO2;
(3)根椐提示可知生成二氧化硫和水,Na2S2O5与稀硫酸反应放出SO2和水,反应的离子方程式为:S2O52-+2H+=2SO2↑+H2O,
故答案为:S2O52-+2H+=2SO2↑+H2O;
(4)反应Ⅰ进行时应先通入氨气,增大HCO3-的浓度,便于NaHCO3析出;上述分析可知,氧化铜与硫酸反应生成硫酸铜,蒸发浓缩,冷却结晶,过滤洗涤,得出硫酸铜晶体,副产品X的化学式是CuSO4•5H2O,根据流程图可知,可循环使用的物质是CO2,
故答案为:NH3;CuSO4•5H2O;CO2;
(5)从生产过程可以看出是硫酸铜晶体;从图示中可以看出二氧化碳和水可以再次利用,反应Ⅱ中气体与固体分别是二氧化硫和碳酸钠,这两种物质反应必须生成亚硫酸氢钠:反应Ⅱ中反应应是二氧化硫与碳酸钠反应生成NaHSO3,NaHSO3再生成Na2S2O5,反应方程式为Na2CO3+2SO2+H2O=2NaHSO3+CO2,因此气体与固体的物质的量之比为2:1,检验产品中含有碳酸钠杂质,需加酸反应检验二氧化碳生成,即用的澄清石灰水,但加酸会生成二氧化硫,二氧化硫也能使澄清石灰水变浑浊,故应先除去,用酸性高锰酸钾溶液根据颜色不褪色确定二氧化硫除净,故选①③⑥,
故答案为:2:1;①③⑥.
点评 本题考查了物质置制备的实验方案分析,主要是物质性质的理解应用,离子方程式书写方法,注意试剂的选择和实验操作的目的,掌握基础是解题关键,题目难度中等.

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案| A. | 新制的氯水在光照下颜色逐渐变浅 | |
| B. | H2、I2、HI平衡混合气缩小体积加压后颜色变深 | |
| C. | 工业上生产硫酸的过程中,SO2在催化氧化时条件控制为常压,而不是高压 | |
| D. | 工业上合成氨气时温度选择450℃左右,而不是常温 |
| A. | 可能含有Fe2+和Fe3+ | B. | 可能含有Fe2+和Cu2+ | ||
| C. | 可能含有Cu2+和Fe3+ | D. | 可能含有单质铜和Fe3+ |
 已知25℃时部分弱电解质的电离平衡常数数据如表所示:
已知25℃时部分弱电解质的电离平衡常数数据如表所示:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | Ka=1.8×10-5 | Kal=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
(1)物质的量浓度均为0.1mol•L-1的四种溶液:a.Na2CO3 b.NaHCO3 c.NaClO d.CH3COONa.它们的pH由大到小排列的顺序是a>c>b>d (填编号).
(2)常温下,0.1mol•L-1CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是BC.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$
C.$\frac{c(O{H}^{-})}{c({H}^{+})}$ D.c(H+)•$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$
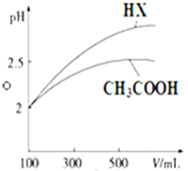
(3)CH3COOH与一元酸HX的溶液均为100mL、pH=2,加水稀释过程中pH与溶液体积的关系如图所示,则同温度时CH3COOH的电离平衡常数小于(填“大于”、“小于”或“等于”) HX的电离平衡常数.
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=9.9×10-7 mol•L-1(保留两位有效数字).
| A. | 实验室制乙酸乙酯时,不断的蒸出乙酸乙酯来提高产率 | |
| B. | CO有毒,会与血液中血红蛋白(用Hb表示)化合发生下述反应:CO+HbO2?HbCO+O2,输氧抢救CO中毒的患者 | |
| C. | 皂化反应采用强碱性条件,促使油脂水解 | |
| D. | 合成氨时,采用高温与高压来提高氨气的产率 |
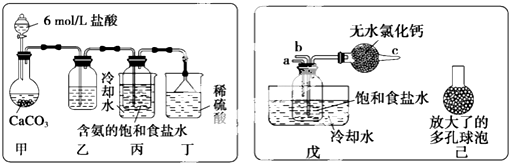
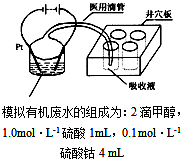 汽车作为一种现代交通工具正在进入千家万户,汽车尾气中含有CO、NO2等有毒气体,其污染问题也成为当今社会急需解决的问题.
汽车作为一种现代交通工具正在进入千家万户,汽车尾气中含有CO、NO2等有毒气体,其污染问题也成为当今社会急需解决的问题.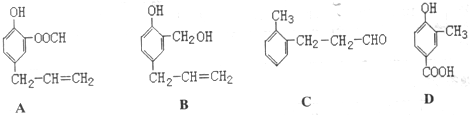
 .
.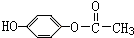 ;H:
;H: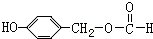 .
.