题目内容
下列有关化学用语正确的是( )
A、NH4Cl的电子式: |
| B、含18个中子的氯原子的核素符号:1735Cl |
C、S2-的结构示意图: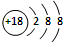 |
| D、次氯酸的结构式:H-O-Cl |
考点:电子式、化学式或化学符号及名称的综合
专题:
分析:A.氯离子为阴离子,氯化铵的电子式需要标出最外层电子;
B.元素符号的左上角表示质量数、左下角表示质量数;
C.硫离子的核电荷数为16,核外电子总数为18;
D.次氯酸中存在1个氢氧键和1个氧氯键.
B.元素符号的左上角表示质量数、左下角表示质量数;
C.硫离子的核电荷数为16,核外电子总数为18;
D.次氯酸中存在1个氢氧键和1个氧氯键.
解答:
解:A.氯化铵为离子化合物,氯离子需要标出最外层电子,氯化铵正确的电子式为: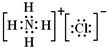 ,故A错误;
,故A错误;
B.含18个中子的氯原子的质量数为35,该核素符号可以表示为:1735Cl,故B错误;
C.硫离子的核电荷数为16,最外层达到8电子稳定结构,硫离子正确的结构示意图为: ,故C错误;
,故C错误;
D.次氯酸为共价化合物,其分子中存在1个1个氢氧键和1个氧氯键,其结构式为:H-O-Cl,故D正确;
故选D.
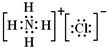 ,故A错误;
,故A错误;B.含18个中子的氯原子的质量数为35,该核素符号可以表示为:1735Cl,故B错误;
C.硫离子的核电荷数为16,最外层达到8电子稳定结构,硫离子正确的结构示意图为:
 ,故C错误;
,故C错误;D.次氯酸为共价化合物,其分子中存在1个1个氢氧键和1个氧氯键,其结构式为:H-O-Cl,故D正确;
故选D.
点评:本题考查了比例模型、电子式、离子结构示意图、结构简式等判断,题目难度中等,注意明确常见的化学用语的概念及正确表示方法,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
MgAgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为:2AgCl+Mg═Mg2++2Ag+2Cl-.有关该电池的说法正确的是( )
| A、可用于海上照明供电 |
| B、负极反应为AgCl+e-═Ag+Cl- |
| C、Mg为电池的正极 |
| D、AgCl为阳极,发生了氧化反应 |
根据下面三个化学方程式判断有关物质的性质比较正确的是( )
①I2+SO2+2H2O=H2SO4+2HI
②2FeCl2+Cl2=2FeCl3
③2FeCl3+2HI=2FeCl2+2HCl+I2.
①I2+SO2+2H2O=H2SO4+2HI
②2FeCl2+Cl2=2FeCl3
③2FeCl3+2HI=2FeCl2+2HCl+I2.
| A、氧化性:I2>H2SO4>Cl2>Fe3+ |
| B、还原性:Cl->Fe2+>SO2>I- |
| C、氧化性:Cl2>Fe3+>I2>H2SO4 |
| D、还原性:SO2>Fe2+>I->Cl- |
下列各组物质相互反应时,水作氧化剂的是( )
①Na和H2O ②Na2O和H2O ③Fe和H2O(g) ④Na2O2和H2O.
①Na和H2O ②Na2O和H2O ③Fe和H2O(g) ④Na2O2和H2O.
| A、①③ | B、①④ | C、②③ | D、②④ |
NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、10g H218O中所含的中子数为5NA |
| B、pH=1的稀硫酸中含有的H+数为0.1NA |
| C、11.2L 的CO气体与0.5molN2所含的电子数相等 |
| D、2L 1mol?L-1 (NH4)2SO4溶液中含有4NA个铵根离子 |
用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A、2 L 1 mol?L-1的盐酸中所含氯化氢分子数为2NA |
| B、1L 0.1 mol?L-1的NaClO溶液中ClO-数目为0.1NA |
| C、标准状况下,11.2L乙醇完全燃烧生成的CO2分子数为NA |
| D、标准状况下,4.48 L N2所含的共用电子对数0.6NA |
下列物质中,物质的量为0.5mol的是( )
| A、27g H2O |
| B、标准状况下,33.6L CO2 |
| C、6.02×1023个O2分子 |
| D、含1mol 氧原子的SO2 |
下列物质,能够直接通过化合反应制取的一组是( )
①FeCl2 ②FeCl3 ③FeS ④Fe(OH)3 ⑤Cu2S ⑥Cu(OH)2 ⑦H2SiO3.
①FeCl2 ②FeCl3 ③FeS ④Fe(OH)3 ⑤Cu2S ⑥Cu(OH)2 ⑦H2SiO3.
| A、②③⑤ | B、①②③⑤ |
| C、①②③④⑤ | D、全部 |