题目内容
MgAgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为:2AgCl+Mg═Mg2++2Ag+2Cl-.有关该电池的说法正确的是( )
| A、可用于海上照明供电 |
| B、负极反应为AgCl+e-═Ag+Cl- |
| C、Mg为电池的正极 |
| D、AgCl为阳极,发生了氧化反应 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:根据电池反应式知,Mg失电子发生氧化反应作负极,负极反应式为Mg-2e-=Mg2+,正极上电极反应式为2AgCl+2e-=2Ag+2Cl-,放电时阴离子向负极移动、阳离子向正极移动,以此解答该题.
解答:
解:A.电池是一种能被海水激活的一次性贮备电池,电池工作时 将化学能转化为电能,电能的产生可用于海上应急照明供电,故A正确;
B.根据电池反应式知,Mg元素化合价由0价变为+2价,则Mg作负极,负极反应式为Mg-2e-=Mg2+,故B错误;
C.Mg被氧化,应为负极反应,故C错误;
D.根据电池反应式中,Ag元素化合价由+1价变为0价,发生还原反应,所以AgCl为电池正极,故D错误.
故选A.
B.根据电池反应式知,Mg元素化合价由0价变为+2价,则Mg作负极,负极反应式为Mg-2e-=Mg2+,故B错误;
C.Mg被氧化,应为负极反应,故C错误;
D.根据电池反应式中,Ag元素化合价由+1价变为0价,发生还原反应,所以AgCl为电池正极,故D错误.
故选A.
点评:本题考查了原电池原理,为高频考点,侧重于学生的分析能力的考查,根据元素化合价确定正负极,再结合离子移动方向、原电池构成条件分析解答,题目难度不大.

练习册系列答案
相关题目
下列实验,在滴加有关试剂之前必须先加碱液使溶液碱化的是( )
| A、乙酸乙酯加水在水浴中加热水解 |
| B、溴苯水解后,滴加硝酸银溶液检验水解产物中的氯离子 |
| C、淀粉水解后,滴加新制氢氧化铜悬浊液检验水解产物中的葡萄糖 |
| D、葡萄糖溶于水,滴加银氨溶液检验其醛基的存在 |
下列有关反应热的叙述正确的是( )
| A、已知2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol,则氢气的燃烧热为241.8kJ/mol |
| B、C(石墨,s)═C(金刚石,s)△H>0,所以金刚石比石墨稳定 |
| C、已知碳的燃烧热为ykJ/mol,当7.2g的碳在12.8g的氧气中燃烧,至反应物耗尽并放出xkJ的热量,则可求出1mol碳与氧气反应生成1mol一氧化碳气体时△H=-(2.5x-0.5y)kJ/mol |
| D、已知2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)═2CO(g)△H2,则△H1>△H2 |
下列有关化学用语正确的是( )
A、NH4Cl的电子式: |
| B、含18个中子的氯原子的核素符号:1735Cl |
C、S2-的结构示意图: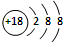 |
| D、次氯酸的结构式:H-O-Cl |
下列离子方程式书写正确的是( )
| A、赤铁矿投入到稀盐酸中:FeO+2H+═Fe2++H2O |
| B、FeCl3溶液中加入氢氧化钠溶液:Fe2++3OH-═Fe(OH)2↓ |
| C、三氯化铁溶液中加入铁粉:2Fe3++Fe═3Fe2+ |
| D、FeCl2溶液跟Cl2反应:Fe2++Cl2═Fe3++2Cl- |
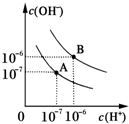 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示: