题目内容
下列物质中,物质的量为0.5mol的是( )
| A、27g H2O |
| B、标准状况下,33.6L CO2 |
| C、6.02×1023个O2分子 |
| D、含1mol 氧原子的SO2 |
考点:物质的量的相关计算
专题:
分析:摩尔质量以g/mol为单位,数值上等于其相对分子质量或相对原子质量,根据n=
、n=
,n=
计算各物质的物质的量,物质的量为0.5mol即为正确选项.
| m |
| M |
| V |
| Vm |
| N |
| NA |
解答:
解:A.27g H2O的物质的量n=
=
=1.5mol,故A错误;
B.标准状况下,33.6L CO2的物质的量n=
=
=1.5mol,故B错误;
C.6.02×1023个O2分子的物质的量n=
=
=1mol,故C错误;
D.根据物质的构成分析,1molSO2含氧原子为2mol,含1mol 氧原子的SO2的物质的量为0.5mol,故D正确;
故选D.
| m |
| M |
| 27g |
| 18g/mol |
B.标准状况下,33.6L CO2的物质的量n=
| V |
| Vm |
| 33.6L |
| 22.4mol/L |
C.6.02×1023个O2分子的物质的量n=
| N |
| NA |
| 6.02×1023 |
| 6.02×1023 |
D.根据物质的构成分析,1molSO2含氧原子为2mol,含1mol 氧原子的SO2的物质的量为0.5mol,故D正确;
故选D.
点评:本题考查物质的量有关计算,侧重微粒数目、物质的构成的计算,比较基础,注意n=
、n=
,n=
计算公式的熟练应用,题目难度不大.
| m |
| M |
| V |
| Vm |
| N |
| NA |

练习册系列答案
相关题目
下列有关化学用语正确的是( )
A、NH4Cl的电子式: |
| B、含18个中子的氯原子的核素符号:1735Cl |
C、S2-的结构示意图: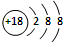 |
| D、次氯酸的结构式:H-O-Cl |
下列溶液中H+浓度为0.01mol/L的是( )
| A、0.01mol/L的CH3COOH |
| B、0.01mol/LNaHSO4 |
| C、0.01mol/LNaHCO3 |
| D、0.005mol/LH2SO3 |
分别取1g左右某脂肪酸(M<300):①与含I2为2.7g的碘的CCl4溶液完全加成;②与含0.2gKOH的溶液所中和.由此推测该脂肪酸的准确相对分子质量可能为( )
| A、290 | B、282 |
| C、280 | D、278 |
在标准状况下,1.12L的某气态单质质量为2.4克,若组成此单质的元素相对原子质量为16,则此单质的相对分子质量及一个分子中含该原子的个数为( )
| A、16和1 | B、32和2 |
| C、48和3 | D、64和4 |
下列离子方程式书写正确的是( )
| A、赤铁矿投入到稀盐酸中:FeO+2H+═Fe2++H2O |
| B、FeCl3溶液中加入氢氧化钠溶液:Fe2++3OH-═Fe(OH)2↓ |
| C、三氯化铁溶液中加入铁粉:2Fe3++Fe═3Fe2+ |
| D、FeCl2溶液跟Cl2反应:Fe2++Cl2═Fe3++2Cl- |
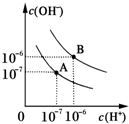 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示:

 请按下列要求填空
请按下列要求填空