题目内容
除去下列物质中所含有的杂质(括号内为杂质),将选用的试剂及分离方法填在题后的横线上,涉及化学反应的并写出有关反应的化学方程式(是离子反应的,写出其离子方程式).
(1)Fe2O3[Fe(OH)3] 、 ;
(2)FeCl3溶液(FeCl2) 、 ;
(3)Fe(Al) 、 .
(4)CO2(SO2) 、 .
(5)SiO2(Al2O3) 、 .
(6)淀粉溶液(氯化钠) .
(7)KNO3(NaCl) .
(8)Br2(H2O) .
(1)Fe2O3[Fe(OH)3]
(2)FeCl3溶液(FeCl2)
(3)Fe(Al)
(4)CO2(SO2)
(5)SiO2(Al2O3)
(6)淀粉溶液(氯化钠)
(7)KNO3(NaCl)
(8)Br2(H2O)
考点:离子方程式的书写,化学方程式的书写
专题:
分析:(1)Fe(OH)3加热分解生成氧化铁;
(2)氯气与FeCl2反应生成氯化铁;
(3)Al与NaOH溶液反应,而Fe不能;
(4)二氧化硫与碳酸氢钠反应,而二氧化碳不能;
(5)氧化铝与盐酸反应,而二氧化硅不能;
(6)分离胶体,选择渗析法;
(7)二者溶解度受温度影响不同;
(8)溴不易溶于水,易溶于有机溶剂.
(2)氯气与FeCl2反应生成氯化铁;
(3)Al与NaOH溶液反应,而Fe不能;
(4)二氧化硫与碳酸氢钠反应,而二氧化碳不能;
(5)氧化铝与盐酸反应,而二氧化硅不能;
(6)分离胶体,选择渗析法;
(7)二者溶解度受温度影响不同;
(8)溴不易溶于水,易溶于有机溶剂.
解答:
解:(1)Fe(OH)3加热分解生成氧化铁,则选择方法为加热,发生的反应为2Fe(OH)3
Fe2O3+3H2O,故答案为:加热;2Fe(OH)3
Fe2O3+3H2O;
(2)氯气与FeCl2反应生成氯化铁,则选择试剂为通入足量的Cl2,发生的离子反应为2Fe2++Cl2═2Fe3++2Cl-,
故答案为:通入足量的Cl2;2Fe2++Cl2═2Fe3++2Cl-;
(3)Al与NaOH溶液反应,而Fe不能则选择试剂和方法为加入过量的NaOH溶液,过滤,发生的离子反应为2Al+2OH-+2H2O═2AlO2-+3H2↑,
故答案为:加入过量的NaOH溶液,过滤;2Al+2OH-+2H2O═2AlO2-+3H2↑;
(4)二氧化硫与碳酸氢钠反应,而二氧化碳不能,则选择饱和碳酸氢钠溶液、洗气,发生的离子反应为2HCO3-+SO2═SO32-+H2O+2CO2↑,
故答案为:饱和碳酸氢钠溶液、洗气;2HCO3-+SO2═SO32-+H2O+2CO2↑;
(5)氧化铝与盐酸反应,而二氧化硅不能,则选择试剂为稀盐酸,离子反应为Al2O3+6H+=2Al3++3H2O,故答案为:稀盐酸;Al2O3+6H+=2Al3++3H2O;
(6)分离胶体,选择渗析法,则需要试剂为蒸馏水,故答案为:渗析法、蒸馏水;
(7)二者溶解度受温度影响不同,则分离二者利用重结晶法,故答案为:重结晶法;
(8)溴不易溶于水,易溶于有机溶剂,则分离出溴,选择苯或四氯化碳等、萃取、分液、蒸馏得到溴,故答案为:苯或四氯化碳等、萃取、分液、蒸馏.
| ||
| ||
(2)氯气与FeCl2反应生成氯化铁,则选择试剂为通入足量的Cl2,发生的离子反应为2Fe2++Cl2═2Fe3++2Cl-,
故答案为:通入足量的Cl2;2Fe2++Cl2═2Fe3++2Cl-;
(3)Al与NaOH溶液反应,而Fe不能则选择试剂和方法为加入过量的NaOH溶液,过滤,发生的离子反应为2Al+2OH-+2H2O═2AlO2-+3H2↑,
故答案为:加入过量的NaOH溶液,过滤;2Al+2OH-+2H2O═2AlO2-+3H2↑;
(4)二氧化硫与碳酸氢钠反应,而二氧化碳不能,则选择饱和碳酸氢钠溶液、洗气,发生的离子反应为2HCO3-+SO2═SO32-+H2O+2CO2↑,
故答案为:饱和碳酸氢钠溶液、洗气;2HCO3-+SO2═SO32-+H2O+2CO2↑;
(5)氧化铝与盐酸反应,而二氧化硅不能,则选择试剂为稀盐酸,离子反应为Al2O3+6H+=2Al3++3H2O,故答案为:稀盐酸;Al2O3+6H+=2Al3++3H2O;
(6)分离胶体,选择渗析法,则需要试剂为蒸馏水,故答案为:渗析法、蒸馏水;
(7)二者溶解度受温度影响不同,则分离二者利用重结晶法,故答案为:重结晶法;
(8)溴不易溶于水,易溶于有机溶剂,则分离出溴,选择苯或四氯化碳等、萃取、分液、蒸馏得到溴,故答案为:苯或四氯化碳等、萃取、分液、蒸馏.
点评:本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应及除杂的考查,题目难度不大.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
在373K 时,把0.5mol N2O4气体通入体积为5L的密闭容器中发生反应:N2O4(g)?2NO2(g).反应进行到2s时,NO2的浓度为0.02mol?L-1.在60s时,体系已达到平衡,此时容器内压强为反应前的1.6倍.下列说法不正确的是( )
| A、平衡时,化学平衡常数K=1.8 |
| B、平衡时,N2O4的转化率为60% |
| C、前2s,N2O4的平均反应速率为0.005mol?L-1?s-1 |
| D、在2s时,体系内压强为反应前的1.1倍 |
已知I2+SO32-+H2O═SO42-+2I-+2H+.某无色溶液中只可能含有I-,NH4+,Ba2+,SO32-,MnO4-中的一种或几种,若向该溶液中滴加少量的溴水,溶液仍为无色,下列判断正确的是( )
| A、该溶液中肯定不含I- |
| B、该溶液中可能含有Ba2+ |
| C、该溶液中肯定含有NH4+ |
| D、该溶液中可能含有MnO4- |
设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A、pH=1的甲酸溶液中,HCOO-和H+ 数目之和为0.1 NA |
| B、标准状况下,3.36L乙烯中含有的非极性键数为0.3NA |
| C、1 mol甲基(-CH3)所含电子数10NA |
D、1mol 含有的双键数目约为5×6.02×1023 含有的双键数目约为5×6.02×1023 |
一定温度下,Wg下列物质在足量氧气中充分燃烧,产物与过量的Na2O2完全反应,Na2O2固体增重Wg,符合此要求的组合是:①H2②CO ③CO和H2 ④HCOOCH3 ⑤HOOC-COOH( )
| A、全部 | B、仅④⑤ |
| C、仅①②③ | D、除⑤外 |
关于Na2O2的叙述正确的是(NA表示阿伏伽德罗常数)( )
| A、7.8g Na2O2含有的共价键数为0.2NA |
| B、7.8 g Na2S与Na2O2的混合物,含离子总数为0.3 NA |
| C、7.8g Na2O2与足量的CO2充分反应,转移的电数为0.2NA |
| D、0.2 mol Na被完全氧化生成7.8g Na2O2,转移电子的数目为0.4NA |
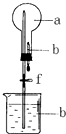 如图装置中,干燥烧瓶中盛满某种气体,烧杯和滴管内盛放某种溶液.挤压滴管的胶头,下列与实验事实不相符的是( )
如图装置中,干燥烧瓶中盛满某种气体,烧杯和滴管内盛放某种溶液.挤压滴管的胶头,下列与实验事实不相符的是( )| A、若a为NO,b为NaOH溶液,可出现无色喷泉 |
| B、若a为HCl,b为AgNO3溶液,可出现白色喷泉 |
| C、若a为CO2,b为NaOH溶液,可出现无色喷泉 |
| D、若a为NH3,b为水(预先滴入少量酚酞溶液),可出现红色喷泉 |