题目内容
一定温度下,有a.盐酸、b.硫酸、c.醋酸三种酸(用a、b、c回答).
(1)当其物质的量浓度相同时.c(H+)由大到小的顺序是 ,pH由大到小的顺序是 .
(2)同体积、同物质的量浓度的三种酸溶液,中和NaOH的能力由大到小的顺序是 .
(1)当其物质的量浓度相同时.c(H+)由大到小的顺序是
(2)同体积、同物质的量浓度的三种酸溶液,中和NaOH的能力由大到小的顺序是
考点:弱电解质在水溶液中的电离平衡
专题:
分析:(1)硫酸为二元酸,盐酸为强酸,醋酸为弱酸;溶液中氢离子浓度越大,pH越小;
(2)同体积同物质的量浓度的三种酸,醋酸和盐酸的物质的量相等,但硫酸为二元酸.
(2)同体积同物质的量浓度的三种酸,醋酸和盐酸的物质的量相等,但硫酸为二元酸.
解答:
解:(1)硫酸为二元酸,盐酸为强酸,醋酸为弱酸,则质的量浓度相同时,c(H+)由大到小的顺序是b>a>c,溶液中氢离子浓度越大,pH越小,则pH由大到小的顺序是c>a>b;
故答案为:b>a>c;c>a>b;
(2)同体积同物质的量浓度的三种酸,醋酸和盐酸的物质的量相等,但硫酸为二元酸,则中和同物质的量浓度的NaOH消耗的体积由大到小的顺序是b>a=c,
故答案为:b>a=c.
故答案为:b>a>c;c>a>b;
(2)同体积同物质的量浓度的三种酸,醋酸和盐酸的物质的量相等,但硫酸为二元酸,则中和同物质的量浓度的NaOH消耗的体积由大到小的顺序是b>a=c,
故答案为:b>a=c.
点评:本题考查了弱电解质的电离,题目难度不大,侧重于基础知识的考查,注意弱酸在溶液中部分电离,其氢离子的浓度小于酸的浓度.

练习册系列答案
相关题目
有Na2CO3、NaHCO3、CaO和NaOH组成的混合物27.2g,把它们溶于足量的水中,充分反应后,溶液中Ca2+、CO32-、HCO3-均转化为沉淀,将反应容器内水分蒸干,最后得白色固体物质共29g,则原混合物中含Na2CO3的质量是( )
| A、10.6 g |
| B、5.3 g |
| C、15.9 g |
| D、无法确定 |
一种从植物中提取的天然化合物其结构为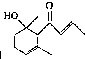 ,可用于制作香水.有关该化合物的下列说法不正确的是( )
,可用于制作香水.有关该化合物的下列说法不正确的是( )
 ,可用于制作香水.有关该化合物的下列说法不正确的是( )
,可用于制作香水.有关该化合物的下列说法不正确的是( )| A、分子式为C12H20O2 |
| B、该化合物可使酸性KMnO4溶液褪色 |
| C、1 mol该化合物完全燃烧消耗15.5mol O2 |
| D、1 mol该化合物可与2mol Br2加成 |
X、Y、Z、W四种短周期元素的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族.下列叙述正确的是( )
| A、元素X只能形成一种氢化物:H2X |
| B、元素W的最高价氧化物对应水化物的酸性比Z的弱 |
| C、原子半径的大小顺序:r(Y)>r(Z)>r(W)>r(X) |
| D、化合物YX、ZX2、WX3中化学键的类型相同 |
下列离子方程式正确的是( )
| A、NH4HCO3溶液中加入少量稀NaOH溶液:NH4++OH-=NH3?H2O |
| B、FeBr2溶液中通入足量的氯气:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
| C、硫酸亚铁溶液中加入用硫酸酸化的双氧水Fe2++2H++H2O2=Fe3++2H2O |
| D、在通入过量SO2后的NaOH溶液中加足量的溴水(不考虑SO2的溶解):HSO3-+Br2+H2O=3H++2Br-+SO42- |
相同物质的量浓度的NaCN和NaClO溶液相比,前者的pH较大,则下列有关同温、同体积和同浓度的HCN和HClO叙述中,正确的是( )
| A、浓度:c(CN-)<c(ClO-) |
| B、pH:HClO>HCN |
| C、酸性:HCN>HClO |
| D、浓度:c(CN-)>c(ClO-) |
室温下,下列有关两种溶液的说法不正确的是( )
| 序号 | ① | ② |
| pH | 12 | 12 |
| 溶液 | 氨水 | 氢氧化钠溶液 |
| A、①②两溶液中c(OH-)相等 |
| B、①溶液的物质的量浓度为0.01 mol?L-1 |
| C、①②两溶液分别加水稀释10倍,稀释后溶液的pH:①>② |
| D、等体积的①②两溶液分别与0.01 mol?L-1的盐酸完全中和,消耗盐酸的体积:①>② |
下列各组物质既不是同系物又不是同分异构体的是( )
| A、甲酸甲酯和乙酸 |
| B、对甲基苯酚和苯甲醇 |
| C、油酸甘油酯和乙酸乙酯 |
| D、软脂酸甘油酯和硬脂酸甘油酯 |