题目内容
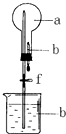 如图装置中,干燥烧瓶中盛满某种气体,烧杯和滴管内盛放某种溶液.挤压滴管的胶头,下列与实验事实不相符的是( )
如图装置中,干燥烧瓶中盛满某种气体,烧杯和滴管内盛放某种溶液.挤压滴管的胶头,下列与实验事实不相符的是( )| A、若a为NO,b为NaOH溶液,可出现无色喷泉 |
| B、若a为HCl,b为AgNO3溶液,可出现白色喷泉 |
| C、若a为CO2,b为NaOH溶液,可出现无色喷泉 |
| D、若a为NH3,b为水(预先滴入少量酚酞溶液),可出现红色喷泉 |
考点:氨的物理性质,氮的氧化物的性质及其对环境的影响
专题:
分析:依据喷泉实验原理:气体极易溶于水或气体与溶液发生化学反应而使气体的体积变小,使烧瓶内外形成负压差,结合物质的性质判断解答.
解答:
解:A.NO与氢氧化钠不反应,也不溶于氢氧化钠溶液,不会产生负压差,不能产生喷泉,故A错误;
B.氯化氢极易溶于水,与硝酸银反应生成白色氯化银沉淀,使瓶内压强迅速减小而产生负压差形成喷泉,氯化银为白色,所以能够形成白色喷泉,故B正确;
C.二氧化碳为酸性氧化物,极易与氢氧化钠溶液反应使烧瓶内压强迅速减小而形成负压差,产生喷泉,碳酸钠溶液为无色,所以喷泉颜色为无色,故C正确;
D.氨气极易溶于水,使烧瓶中的气压减小,且小于外界大气压,则形成喷泉,又氨水溶液显碱性,石蕊遇碱变蓝,故形成蓝色喷泉,故D正确;
故选:A.
B.氯化氢极易溶于水,与硝酸银反应生成白色氯化银沉淀,使瓶内压强迅速减小而产生负压差形成喷泉,氯化银为白色,所以能够形成白色喷泉,故B正确;
C.二氧化碳为酸性氧化物,极易与氢氧化钠溶液反应使烧瓶内压强迅速减小而形成负压差,产生喷泉,碳酸钠溶液为无色,所以喷泉颜色为无色,故C正确;
D.氨气极易溶于水,使烧瓶中的气压减小,且小于外界大气压,则形成喷泉,又氨水溶液显碱性,石蕊遇碱变蓝,故形成蓝色喷泉,故D正确;
故选:A.
点评:本题考查了喷泉实验,明确喷泉实验的原理和物质的性质是解题关键,题目难度不大.

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目
下列各组物质既不是同系物又不是同分异构体的是( )
| A、甲酸甲酯和乙酸 |
| B、对甲基苯酚和苯甲醇 |
| C、油酸甘油酯和乙酸乙酯 |
| D、软脂酸甘油酯和硬脂酸甘油酯 |
下列过程或现象与盐类水解无关的是( )
| A、可用碳酸钠与醋酸制取少量二氧化碳 |
| B、泡沫灭火器用碳酸氢钠溶液和硫酸铝溶液,使用时只需将其混合就可产生大量二氧化碳的泡沫 |
| C、厨房中常用碳酸钠溶液洗涤餐具上的油污 |
| D、实验室盛放碳酸钠溶液的试剂瓶必须用橡胶塞而不能用玻璃塞 |
常温时,下列溶液的pH或微粒的物质的量浓度关系不正确的是( )
| A、将0.2 mol?L-1的某一元酸HA溶液和0.1 mol?L-1 NaOH溶液等体积混合后,混合液pH大于7,则反应后的混合液:2c(OH一)+c(A-)═2c(H+)+c(HA) |
| B、某溶液中存在的离子有Cl-、OH-、NH4+、H+,则离子浓度不一定是c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C、某物质的溶液中由水电离出的c(H+)=1×10-a mol?L-1,若a>7时,则该溶液的pH一定为14-a |
| D、pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液:2c(R2-)+c(HR一)=c(Na+) |
对已达化学平衡的反应:2X(g)+Y(g)?2Z(g),减小压强后,对反应产生的影响是( )
| A、逆反应速率增大,正反应速率减小,平衡向逆反应方向移动 |
| B、逆反应速率减小,正反应速率增大,平衡向正反应方向移动 |
| C、正反应速率先减小后增大,逆反应速率减小,平衡向逆反应方向移动 |
| D、逆反应速率先减小后增大,正反应速率减小,平衡向逆反应方向移动 |
在恒容绝热(不与外界交换能量)条件下进行2A(g)+B(g)?2C(g)+D(s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高.下列叙述正确的是( )
| 物 质 | A | B | C | D |
| 起始投料/mol | 2 | 1 | 2 | 0 |
| A、该反应是吸热反应 |
| B、该反应的平衡常数随温度的升高而增大 |
| C、压强升高时平衡常数也随之增大 |
| D、该反应的平衡常数随温度的升高而减小 |
下列离子方程式正确的是( )
| A、金属钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
| B、金属铝投入NaOH溶液中:Al+2OH-=AlO2-+H2↑ |
| C、稀硝酸中加入过量铁粉:Fe+4H++NO3-=Fe3++NO↑+2H2O |
| D、FeCl2酸性溶液放在空气中变质:4Fe2++4H++O2=4Fe3++2H2O |
 根据如图所示装置回答问题:
根据如图所示装置回答问题: